题目内容
【题目】下列事实一定能说明HF是弱酸的是( )
①常温下NaF溶液的pH大于7;②用HF溶液做导电性实验,灯泡很暗;③等物质的量浓度的HCl溶液和HF溶液与足量锌粒反应,刚开始HCl溶液产生的气泡快;④常温下0.1mol/L的HF溶液pH为2.3;⑤HF能与Na2CO3溶液反应,产生CO2气体;⑥HF与水能以任意比混溶;⑦1mol/L的HF水溶液能使紫色石蕊试液变红;⑧pH=3的HF溶液稀释至原体积的10倍,pH值减小0.6;⑨等物质的量浓度的HCl溶液和HF溶液与足量锌粒反应,产生氢气的量一样多
A.①③④B.①②③④⑤⑧C.②④⑧⑨D.①②⑦⑧
【答案】A
【解析】
①常温下NaF溶液的pH大于7,说明F-能发生水解,一定能说明HF是弱酸;
②用HF溶液做导电性实验,灯泡很暗,因为没有与相同条件下的强酸进行对比,不能说明HF是弱酸;
③等物质的量浓度的HCl溶液和HF溶液与足量锌粒反应,刚开始HCl溶液产生的气泡快,说明在盐酸中![]() 较大,而HF溶液中
较大,而HF溶液中![]() 较小,故一定能说明HF是弱酸;
较小,故一定能说明HF是弱酸;
④常温下0.1mol/L的HCl的pH为1,而0.1mol/L的HF溶液pH为2.3,说明HF没有完全电离,故一定能说明HF是弱酸;
⑤HF能与Na2CO3溶液反应,产生CO2气体,只能说明其有酸性且酸性强于碳酸,但是不能说明HF是弱酸;
⑥HF与水能以任意比混溶,说明了HF的溶解性好,但不能说明HF是弱酸;
⑦1mol/L的HF水溶液能使紫色石蕊试液变红,只能说明其有酸性,但是不能说明HF是弱酸;
⑧pH=3的强酸稀释至原体积的10倍,pH值将增大1个单位。pH=3的HF溶液稀释至原体积的10倍,pH值减小0.6,不能说明HF是弱酸;
⑨等物质的量浓度的HCl溶液和HF溶液与足量锌粒反应,产生氢气的量一样多,只能说明两种一元酸的物质的量相同,不能说明HF是弱酸。
综上所述,一定能说明HF是弱酸的是①③④,故选A。

【题目】酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是碳粉,MnO2,ZnCl2和NH4Cl等组成的糊状填充物,该电池在放电过程产生MnOOH,回收处理该废电池可得到多种化工原料,有关数据下表所示:
溶解度/(g/100g水)
温度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp近似值 | 10-17 | 10-17 | 10-38 |
回答下列问题:
(1)该电池的正极反应式为___,电池反应的离子方程式为:___。
(2)维持电流强度为0.5A,电池工作十分钟,理论上消耗Zn___g。(已经F=96500C/mol)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有ZnCl2和NH4Cl,二者可通过__分离回收;滤渣的主要成分是MnO2、___和___,欲从中得到较纯的MnO2,最简便的方法是在空气中加热,其原理是___。
(4)用废电池的锌皮制备ZnSO4·7H2O的过程中,需去除少量杂质铁,其方法是:加稀硫酸和H2O2溶解,铁变为__,加碱调节至pH为__时,铁刚好完全沉淀;继续加碱调节至pH为___时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。若上述过程不加H2O2后果是___,原因是__。
【题目】如图是元素周期表的一部分,按要求回答问题:
① |
| ||||||||||||||||
|
|
| ② | ③ | ④ |
|
| ||||||||||
⑤ | ⑥ |
|
|
|
|
|
|
|
|
|
| ⑦ |
|
| ⑧ | ⑨ |
|
(1)元素④在周期表中位置是_______。元素③的最高价氧化物的化学式为________。
(2)元素①⑤组成化合物电子式为___________。
(3)元素②的单质与⑧的最高价氧化物的水化物热的浓溶液反应的化学方程式为___。
(4)元素⑦与⑨形成的化合物与元素③的氢化物的水溶液反应的离子方程式为_____。
(5)元素④⑤⑥⑧形成的简单离子,其离子半径由小到大的顺序为_____(用离子符号表示)。
(6)A—F发生如图所示的转化,A、B、C、D为①—⑨中某种元素形成的单质,E、F、G为B、C、D与A形成的二元化合物,G是一种常见温室气体,与B可以反应生成E,E中B元素的质量分数为60%,F为两性物质。
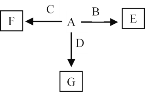
①A和F的化学式分别为_______、_______。
②B与G反应的化学方程式为____________________。
③C与NaOH溶液反应的离子方程式为______________。