题目内容
下列物质的变化过程中,化学键没有被破坏的是( )
| A.食盐溶解 | B.干冰升华 | C.氯化铵受热 | D.氯化钠熔融 |
B
解析试题分析:A、食盐溶解破坏了氯化钠中的离子键,错误;B、干冰升华只克服了分子间作用力,正确;C、氯化铵受热破坏了离子键,错误;D、氯化钠熔融破坏了离子键,错误。
考点:在物质发生物理或化学变化过程中化学键的变化。

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
下列反应既是氧化还原反应,又是吸热反应的是( )
| A.铝片和稀硫酸反应 | B.Ba(OH)2?8H2O与NH4Cl反应 |
| C.灼热的炭与CO2反应 | D.甲烷在O2中燃烧 |
能将化学能转化为热能的是
| A.光合作用 | B.水力发电 | C.燃煤取暖 | D.燃料电池 |
下列图像分别表示有关反应的反应过程与能量变化的关系
据此判断下列说法中正确的是( )
| A.白磷比红磷稳定 |
| B.石墨转变为金刚石是吸热反应 |
| C.S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g);△H2则△H1>△H2 |
| D.CO(g)+H2O(g)=CO2(g)+ H2 (g);△H1>0 |
一定条件下,发生反应:①M(s)+N(g)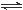 R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g)
R(g) △H = -Q1 kJ·mol-1,②2R (g)+N(g)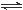 2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2、Q3均为正值。下列说法正确的是
2T (g) △H = -Q2 kJ·mol-1。 Q1、Q2、Q3均为正值。下列说法正确的是
| A.1 mol R(g)的能量总和大于1 mol M(s)与1 mol N(g) 的能量总和 |
| B.将2 mol R (g)与1 mol N(g)在该条件下充分反应,放出热量Q2 kJ |
C.当1 mol M(s)完全转化为T (g)时(假定无热量损失),放出热量Q1+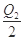 kJ kJ |
D.M(g)+N(g)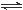 R(g) △H=-Q3 kJ·mol-1 , 则Q3<Q1 R(g) △H=-Q3 kJ·mol-1 , 则Q3<Q1 |
氢能是理想的清洁能源。下列制氢的方法中,最节能的是
| A.电解水制氢:2H2O电解2H2↑+O2↑ |
| B.高温使水分解制氢:2H2O高温2H2↑+O2↑ |
C.太阳光催化分解水制氢:2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
| D.天然气制氢:CH4+H2O高温CO+3H2 |
下列说法不正确的是( )
| A.煤经过气化和液化等物理变化可以转化为清洁燃料 |
| B.侯氏制碱法的工艺过程,应用了物质溶解度的差异 |
| C.食品包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同 |
| D.甘氨酸和丙氨酸发生脱水反应,最多可生成4种二肽 |
下列说法不正确的是
A.已知H2(g)+ O2(g)===H2O(g) ΔH1=a kJ·mol-1; O2(g)===H2O(g) ΔH1=a kJ·mol-1;2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1,则a>b |
| B.CO的燃烧热为283.0 kJ·mol-1,则 2CO2(g)===2CO(g)+O2(g) ΔH=+566.0 kJ·mol-1 |
C.若N2(g)+3H2(g)  2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ 2NH3(g) ΔH=-d kJ·mol-1,故在某容器中投入1 mol N2与3 mol H2充分反应后,放出的热量小于d kJ |
| D.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和KOH反应的中和热ΔH=-114.6 kJ·mol-1 |
