题目内容
【题目】在Cu+HNO3 ———— Cu(NO3)2+NO↑+4H2O反应中,
(1) ______ 元素被氧化, ______ 是氧化剂;
(2) ______ 是氧化产物, ______ 发生氧化反应;
(3)被还原的HNO3与参加反应的HNO3物质的量之比是 ______;
(4)用双线桥标出该反应电子转移的方向和数目:
3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O _____________________________________;
(5)当有8mol HNO3被还原时,反应转移___________个电子;
(6)写出该反应的离子反应方程式___________________________。
【答案】铜 HNO3 Cu(NO3)2 Cu 1:4 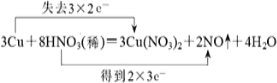 24NA 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
24NA 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
【解析】
该反应中Cu元素化合价由0价变为+2价、部分N元素化合价由+5价变为+2价,其得失电子最小公倍数是6,所以铜是还原剂、部分硝酸是氧化剂,还原剂发生氧化反应、氧化剂发生还原反应,据此分析解答;
(1)该反应中Cu元素失电子被氧化,HNO3中部分N元素被还原,故HNO3是氧化剂;
答案为:铜;HNO3;
(2)该反应中铜是还原剂,则氧化产物是Cu(NO3)2,还原剂发生氧化反应,所以铜发生氧化反应;
答案为:Cu(NO3)2;Cu;
(3)配平后的方程式为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,被还原的硝酸是生成NO的硝酸,则被还原的HNO3与参加反应的HNO3物质的量之比为2:8=1:4;
答案为:1:4;
(4)该反应中Cu元素化合价由0价变为+2价、部分N元素化合价由+5价变为+2价,其得失电子最小公倍数是6,用双线桥标出该反应电子转移的方向和数目为: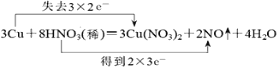 ;
;
答案为: ;
;
(5)作氧化剂的HNO3中N元素化合价由+5价变为+2价,故有8mol HNO3被还原时,转移电子数为:8mol×3×NA mol-1=24NA;
答案为:24NA;
(6)硝酸为一元强酸,硝酸铜为可溶性盐,书写离子反应方程式时拆分,故该反应的离子反应方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案