��Ŀ����
����Ŀ��ij��糧�ղ����ķ�ú�ҵ���Ҫ�ɷ�ΪSiO2��Al2O3��FeO��Fe2O3��MgO��TiO2�ȡ��о�С���������ۺϴ������������£�
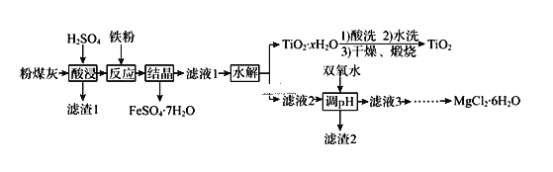
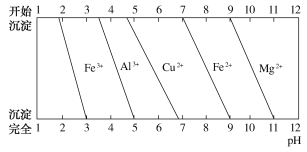
��֪���������£�Ksp[Al(OH)3] �� 8.0��10-35������Һ1������Fe2+ʣ���Fe3+��ȫ����ʱpHΪ3.7��Al3+��ȫ����ʱpHΪ5.0��Fe2+��ȫ����ʱpHΪ9.7��
��1��Ϊ����߷�ú�ҽ������ʣ����������ʱ�ɲ�ȡ�Ĵ�ʩ��_________����д���֣���
��2�������ж�TiO2xH2O�����Ѿ�ϴ�Ӹɾ�________________________________��
��3������˫��ˮ��Ŀ����_____________________________________������2�еijɷֱַ�ΪAl(OH)3��_______________��Al(OH)3������ȫʱ(��Һ������Ũ��С��10-5mol/L)����Һ�е�c(OH-)Ϊ________��
��4����MgCl26H2O�Ƴ���ˮMgCl2ʱӦע��__________________________________��
��5��ijͬѧ��ʯīΪ�����缫�����MgCl2��Һ����ȡ����þ������Ϊ���ܷ��óɹ���_______���û�ѧ����ʽ����ԭ��___________________________________��
���𰸡��ʵ������¶ȣ��ʵ����������Ũ�ȣ������,ȡ���һ��ϴ��Һ������ϡ���ᣬ���������� �ټ����Ȼ�����Һ��û�а�ɫ�������ɣ�����ж��Ѿ�ϴ�Ӹɾ�����Ҳ���Լ���Mg2+��Fe2+��Al3+���� ��Fe2+������Fe3+�������γ�Fe(OH)3�������ﵽ��ȥ��Ԫ�����ʵ�Ŀ�� Fe(OH)3 2��10-10 ��HCl�����ı����£����������ᣩ��С�ļ��� �� MgCl2 + 2H2O![]() MgOH)2��+ H2��+ Cl2��
MgOH)2��+ H2��+ Cl2��
��������
�ӹ������̿�����ú���ۺ������Ƶ�FeSO4��7H2O��TiO2��MgCl2��6H2O���ʺ���Ԫ���������ѡ�þ���֣�SiO2��Al2O3Ϊ���ʣ������ȥ�����������ʵ��Ʊ�Ϊ���ģ�����������ÿһ�������Ļ�ѧ��Ӧ������ÿһ��������Ŀ�ģ��Ӷ��ش����⡣
��1���������ʱ��ϡ�������ú�����ã���SiO2�Ȳ����⣬����ܽ⣬����1ΪSiO2�ȡ���߷�ú�ҽ�����Ӧ���ʣ�Ӧ��Ӱ�췴Ӧ���ʵ����ؿ��ǣ����Խ���ʹ��Һ��ֽӴ����ʵ������¶ȡ��ʵ����������Ũ�ȵȡ�
��2����Һ1��ˮ��������TiO2xH2O������TiO2xH2O���������������������Ե�MgSO4��Al2(SO4)3������FeSO4�ȡ��ж�TiO2xH2O�����Ѿ�ϴ�Ӹɾ�����ͨ��ʵ��֤����������Ѿ���SO42���������ǣ�ȡ���һ��ϴ���˳���Һ���������μ�ϡ�����ữ�������������ٵμ��Ȼ�����Һ��û�а�ɫ�������ɣ����Ѿ�ϴ�Ӹɾ���
��3����Һ2����MgSO4��Al2(SO4)3������FeSO4�ȣ�����˫��ˮ��Fe2+����ΪFe3+�������γ�Fe(OH)3�������ﵽ����Ŀ�ġ��ٵ���pHΪ5.0ʹFe3+��Al3+��ȫ������������2ΪAl(OH)3��Fe(OH)3����Al(OH)3(s)![]() Al3++3OH����Ksp[Al(OH)3] ��c(Al3+)��c3(OH��)���������ݵ�c(OH��)��
Al3++3OH����Ksp[Al(OH)3] ��c(Al3+)��c3(OH��)���������ݵ�c(OH��)��![]() ��2��10-10mol��L-1��
��2��10-10mol��L-1��
��4��ֱ�Ӽ���MgCl26H2O����ȫˮ�⣺MgCl26H2O![]() Mg(OH)2+2HCl��+4H2O����HCl�����м�����ˮ������ˮ�⣬�Ƶ���ˮMgCl2��
Mg(OH)2+2HCl��+4H2O����HCl�����м�����ˮ������ˮ�⣬�Ƶ���ˮMgCl2��
��5����ʯīΪ�缫���MgCl2��Һ��������Ӧ2Cl-��2e-=Cl2����������ӦΪ2H2O+2e-=H2��+2OH�����ܷ�Ӧ��ѧ����ʽMgCl2 + 2H2O![]() MgOH)2��+ H2��+ Cl2�����ʵ��MgCl2��Һ�����Ƶý���þ����ҵ�ϳ���������Ȼ�þ��ȡ����þ��
MgOH)2��+ H2��+ Cl2�����ʵ��MgCl2��Һ�����Ƶý���þ����ҵ�ϳ���������Ȼ�þ��ȡ����þ��

����Ŀ��ij��ҵ��ˮ�н������е������е�5�֣�������ˮ�ĵ��뼰���ӵ�ˮ�⣩���Ҹ������ӵ����ʵ���Ũ����ȣ���Ϊ0.1mol/L��
������ | K+ Cu2+ Fe3+ Al3+ Fe2+ |
������ | Cl�� CO32- NO3�� SO42�� SiO32�� |
��ͬѧ��̽����ˮ����ɣ�����������ʵ�飺
I.�ò�˿պȡ������Һ���ڻ��������գ�����ɫ���棨����ɫ�ܲ����۲죩��
��.ȡ������Һ������KSCN��Һ�����Ա仯��
��.��ȡ��Һ�����������ᣬ����ɫ�������ɣ�����ɫ������������ɺ���ɫ����ʱ��Һ��Ȼ���壬����Һ������������䡣
��.��������õ���Һ�м���BaCl2��Һ���а�ɫ�������ɡ�
���ƶϣ�
(1)���м�����������������ɫ��������ӷ���ʽ��____________________��
(2)�����к���ɫ���壨����£��ռ�һ���Թ�Ȼ����ˮ�У��������ʲ���ɢ����������Һ�����ʵ���Ũ��Ϊ___________mol/L����ȷ��ǧ��λ����
(3)��ͬѧ����ȷ��ԭ��Һ������������__________________��
(4)��ȡ100mLԭ��Һ������������NaOH��Һ����ַ�Ӧ����ˣ�ϴ�ӣ����������أ��õ��Ĺ�������Ϊ_____________g��
����Ŀ���������ڵ�Cr��Fe��Co��Ni��Cu��Zn������������γ��������������鼰���ǵĻ�����㷺Ӧ���ڳ�������ϵ�������ش��������⣺
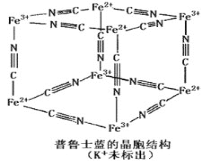
��1��Fe2+�ĺ�������Ų�ʽΪ_________________��
��2��NH3��һ�ֺܺõ����壬NH3�ķе�______(����>����=������<��)AsH3��
��3��Nԭ�Ӻ�����______�ֲ�ͬ�˶�״̬�ĵ��ӡ���̬Nԭ���У�������ߵĵ�����ռ�ݵ�ԭ�ӹ������״Ϊ_____��
��4����ѧ��ͨ��X���߲�õ����ṹʾ��ͼ�ɼ�ʾ��ͼ��ͼ�����߱�ʾ��������Ϊ________��
��5��As��±������۵����£�
AsCl3 | AsBr3 | AsI3 | |
�۵�/K | 256.8 | 304 | 413 |
����±�����۵�����ԭ����________________��
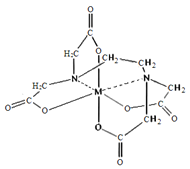
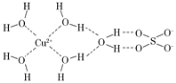
��6����FeCl3��Һ�е���EDTA�Լ��ɵ������A,��ṹ��ͼ��ʾ��ͼ��M����Fe3+����Fe3+�뵪ԭ��֮���γɵĻ�ѧ����_______��Fe3+����λ��Ϊ______��