题目内容
5.关于下列各实验装置的叙述中,不正确的是( )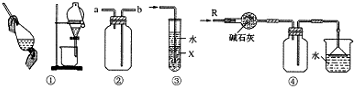
| A. | 装置①可用于分离苯和水的化合物 | |
| B. | 装置②可用于排气法收集H2、CO2、Cl2、NO、NO2等气体 | |
| C. | 装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 | |
| D. | 装置④可用于干燥、收集NH3,并吸收多余的NH3 |
分析 A.苯与水混合分层;
B.NO与氧气反应,不能使用排空气法收集;
C.X若为CCl4,密度比水大,水在上方,使气体与水不能直接接触;
D.氨气不与碱石灰反应,密度比空气小,且极易溶于水.
解答 解:A.苯与水混合分层,可利用图中分液漏斗分离,故A正确;
B.NO与氧气反应,不能使用排空气法收集,而a进入可收集H2,b进气可收集CO2、Cl2、NO2,故B错误;
C.X若为CCl4,密度比水大,水在上方,使气体与水不能直接接触,则图中装置可用于吸收NH3或HCl,并防止倒吸,故C正确;
D.氨气不与碱石灰反应,可干燥气体,密度比空气小,图中向下排空气法收集合理,且极易溶于水,图中倒扣的漏斗可防止倒吸,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、气体的收集、气体制备及防倒吸装置等,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
15.下列各组物质中,最简式相同,但既不是同系物,又不是同分异构体的是( )
| A. | 丙烯、环丙烷 | B. | 乙酸、甲酸甲酯 | C. | 乙烯、1-丁烯 | D. | 甲醛、甲酸甲酯 |
16.某溶液中仅含有以下离子中的五种(不考虑水的电离和离子的水解),且各离子的物质的量浓度相等.阳离子:Na+、Mg2+、Fe2+、Al3+、Fe3+;阴离子:OH-、CO32-、Cl-、NO3-、SO42-.下列说法正确的是( )
| A. | 溶液中肯定不存在.的离子是Na+和CO32- | |
| B. | 用氢氧化钠溶液可以确定阳离子的组成 | |
| C. | 溶液中加入稀硫酸,有气体产生 | |
| D. | 溶液中存在的Cl-,可用硝酸酸化的硝酸银溶液检验 |
13.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1.6g甲烷含有的电子数为NA | |
| B. | 1 L0.1 mol/L NaHCO3溶液中含有的HCO3- 数目为0.1 NA | |
| C. | 1 L PH=1的硫酸溶液中含有的H+ 数为0.2 NA | |
| D. | 标准状况下,2.24 LCO和CO2混合气体中含有的氧原子数为0.15NA |
20.常温下,对于pH=11的NaOH溶液,下列说法错误的是( )
| A. | c(OH-)=c(Na+)+c(H+) | |
| B. | 该溶液中的c(OH-)=1.0x10-3mol•L-1 | |
| C. | 加水稀释104倍所得溶液显碱性 | |
| D. | 与pH=3的HF溶液等体积混合所得溶液:c(Na+)=c (F-)+c(HF) |
10.下列装置所示的实验中,能够达到实验目的是( )
| A. |  用铜和稀硝酸制取NO | B. |  分离乙醇和乙酸 | ||
| C. | 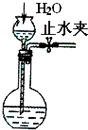 检查装置气密性 | D. | 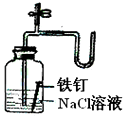 证明铁生锈空气参与反应 |
17.分子式为为C9H11Br,且苯环上有两个取代基的芳香族化合物,其可能的结构有(不考虑立体异构)( )
| A. | 5种 | B. | 9种 | C. | 12种 | D. | 15种 |
14.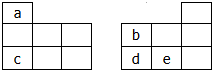 如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.
如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.
 如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.
如图均为元素周期表短周期的一部分,其中b的氢化物和它的最高价氧化物对应的水化物能反应生成盐,下列有关a、b、c、d、e五种元素的叙述中,正确的是(0.| A. | 原子半径:b>c | |
| B. | 由a、b、e三种元素形成的化合物可能是离子化合物 | |
| C. | c与e以原子个数比2:1形成的化合物能促进水的电离 | |
| D. | 氢化物的稳定性:b<d. |
13.下列有关化学用语正确的是( )
| A. | 乙烯的最简式:C2H4 | B. | 乙醛分子的结构简式是CH3COH | ||
| C. | 四氯化碳的电子式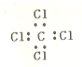 | D. | 苯的分子式C6H6 |