题目内容
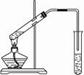
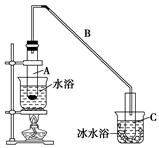
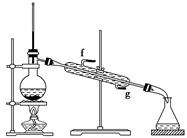
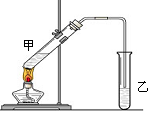
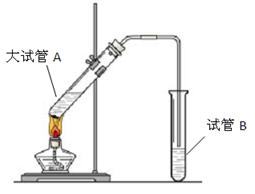
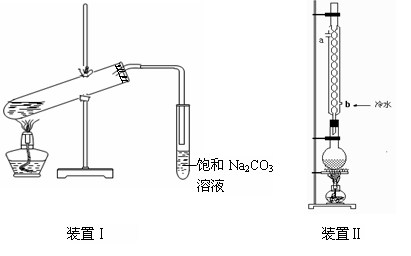
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制取乙酸乙酯。回答下列问题:
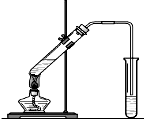
⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
A加成反应 B取代反应 C水解反应 D酯化反应 E可逆反应
⑶酯化反应的断键特点是:
⑷写出制取乙酸乙酯的化学反应方程式:
⑸为了证明浓硫酸的作用,某同学进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡小试管Ⅱ再测有机物的厚度,实验记录如表:
实验D的目的是与实验C对照,证明H+对该反应的催化作用。实验D中加入盐酸的体积和浓度分别是 mL和 mol/L。

⑴装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
⑵该反应属于哪类反应类型 。
A加成反应 B取代反应 C水解反应 D酯化反应 E可逆反应
⑶酯化反应的断键特点是:
⑷写出制取乙酸乙酯的化学反应方程式:
⑸为了证明浓硫酸的作用,某同学进行了以下4个实验。实验开始先用酒精灯微热3 min,再加热使之微微沸腾3 min。实验结束后充分振荡小试管Ⅱ再测有机物的厚度,实验记录如表:
| 实验编号 | 试管Ⅰ中试剂 | 试管Ⅱ中试剂 | 有机层厚度/cm |
| A | 3 mL乙醇、2 mL乙酸、1 mL 18 mol/L浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3 mL乙醇、2 mL乙酸 | 饱和Na2CO3溶液 | 0.1 |
| C | 3 mL乙醇、2 mL乙酸、6 mL 3 mol/L硫酸 | 饱和Na2CO3溶液 | 1.2 |
| D | 3 mL乙醇、2 mL乙酸、一定浓度的盐酸 | 饱和Na2CO3溶液 | 1.2 |
⑴倒吸 ⑵BDE ⑶酸脱羟基醇脱氢基
⑷CH3COOH+CH3CH2OH CH3COOC2H5+H2O ⑸6;6
CH3COOC2H5+H2O ⑸6;6
⑷CH3COOH+CH3CH2OH
 CH3COOC2H5+H2O ⑸6;6
CH3COOC2H5+H2O ⑸6;6 试题分析:⑴因为通入的物质含有乙醇和乙酸这些易溶物质,所以装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,是为了防止倒吸;⑵该反应属于酯化反应,同时是取代反应和可逆反应,所以该题选择BDE;⑶酯化反应的断键特点是:酸脱羟基醇脱氢基;⑷制取乙酸乙酯的化学反应方程式为:CH3COOH+CH3CH2OH
 CH3COOC2H5+H2O;⑸实验D的目的是与实验C对照,证明H+对该反应的催化作用,对比CD可以知道除了浓度为其他的应该都一样,所以实验D中加入盐酸的体积和浓度分别是6mol/L、6mol/L。
CH3COOC2H5+H2O;⑸实验D的目的是与实验C对照,证明H+对该反应的催化作用,对比CD可以知道除了浓度为其他的应该都一样,所以实验D中加入盐酸的体积和浓度分别是6mol/L、6mol/L。点评:本题考查了酯化反应,酯化反应是高中经典的实验之一,是高考的常考考点,本题难度适中。

练习册系列答案
相关题目