题目内容
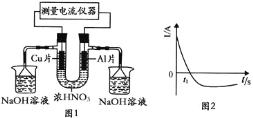
【题目】可以将氧化还原反应2H2+O2![]() 2H2O设计成原电池。
2H2O设计成原电池。
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,电极反应式为:正极_________,负极______________。
(2)如果把KOH改为稀硫酸作电解质,则电极反应式为:正极:____________。
(3)(1)和(2)的电解质溶液不同,反应进行后,其溶液的pH各有何变化?__________。
(4)如把H2改为甲烷,KOH溶液作电解质溶液,则电极反应式为:正极:__________,负极:__________。
【答案】O2+2H2O+4e-=4OH- 2H2+4OH--4e-=4H2O O2+4H++4e-=2H2O 前者变小,后者变大 2O2+4H2O+8e-=8OH- CH4+10OH--8e-=CO32-+7H2O
【解析】
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,正极的电极反应式为O2 + 2H2O + 4e- =4OH-,负极的电极反应式为:2H2 - 4e- + 4OH- =4H2O;
(2)若把KOH改为稀硫酸作电解质,正极的电极反应式为O2 + 4H+ + 4e- =2H2O,负极的电极反应式为:2H2 - 4e-=4H+;
(3)利用该反应2H2+O2![]() 2H2O设计的原电池,都生成水,因此电解质溶液浓度减小;
2H2O设计的原电池,都生成水,因此电解质溶液浓度减小;
(4)如把H2改为甲烷,KOH溶液作电解质溶液,则电极反应式为:正极: 2O2+4H2O+8e-=8OH-;负极:CH4+10OH--8e-=CO32-+7H2O。
(1)利用氢气和氧气、氢氧化钾溶液构成燃料电池,氢气在负极失电子发生氧化反应,氧气在正极得电子发生还原反应,正极的电极反应式为O2 + 2H2O + 4e- =4OH-,负极的电极反应式为:2H2 - 4e- + 4OH- =4H2O;
故答案为:O2+2H2O+4e-=4OH-;2H2+4OH--4e-=4H2O;
(2)若把KOH改为稀硫酸作电解质,正极的电极反应式为O2 + 4H+ + 4e- =2H2O,负极的电极反应式为:2H2 - 4e-=4H+;
故答案为:O2+4H++4e-=2H2O;
(3)利用该反应2H2+O2![]() 2H2O设计的原电池,都生成水,因此电解质溶液浓度减小,氢氧化钾溶液浓度减小,pH变小,稀硫酸浓度减小,pH变大;
2H2O设计的原电池,都生成水,因此电解质溶液浓度减小,氢氧化钾溶液浓度减小,pH变小,稀硫酸浓度减小,pH变大;
故答案为:前者变小,后者变大;
(4)如把H2改为甲烷,KOH溶液作电解质溶液,甲烷在负极失电子发生氧化反应,氧气在正极得电子发生还原反应,则电极反应式为:正极: 2O2+4H2O+8e-=8OH-;负极:CH4+10OH--8e-=CO32-+7H2O;
故答案为:2O2+4H2O+8e-=8OH-;CH4+10OH--8e-=CO32-+7H2O。

 阅读快车系列答案
阅读快车系列答案【题目】某同学用已知物质的量浓度的NaOH测定未知物质的量浓度的盐酸,将20.00 ![]() 待测盐酸放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2-3次,记录数据如下。
待测盐酸放入锥形瓶中,并滴加2-3滴酚酞作指示剂,用NaOH标准溶液进行滴定。重复上述滴定操作2-3次,记录数据如下。
实验编号 |
| 滴定完成时, | 待测盐酸的体积/ |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
① 滴定达到终点的标志是____________________________。
② 根据上述数据,可计算出该盐酸的浓度约为_______(保留两位有效数字)。
③ 排除碱式滴定管中气泡的方法应采用如图所示操作中的________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

④ 在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________(填字母序号)。
A. 滴定终点读数时俯视
B. 酸式滴定管使用前,水洗后未用待测盐酸润洗
C. 锥形瓶水洗后未干燥
D. 称量的![]() 固体中混有
固体中混有![]() 固体
固体
E. 碱式滴定管尖嘴部分有气泡,滴定后消失