题目内容
用CH4催化还原NOx可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
下列说法不正确的是( )
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
下列说法不正确的是( )
| A、反应①②均为放热反应 | B、反应①②转移的电子数相同 | C、由反应①可推知:CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H=-akJ?mol-1,a<574 | D、著用标准状况下4.48L CH4还原NO2至N2,放出的热量是173.4kJ |
分析:A.根据方程式中△H符号判断;
B.根据元素化合价变化判断;
C.水蒸气液化放出热量;
D.根据甲烷和反应热的关系式计算.
B.根据元素化合价变化判断;
C.水蒸气液化放出热量;
D.根据甲烷和反应热的关系式计算.
解答:解:A.由方程式中△H符号可知,△H均为负值,所以都是放热反应,故A正确;
B.等物质的量的甲烷分别参加反应①、②时,碳元素的化合价变化相同,所以反应转移的电子数相同,故B正确;
C.水蒸气液化放出热量,所以生成液态水放出热量多,所以得CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H=-akJ?mol-1,a>574,故C错误;
D.用标准状况下4.48L CH4还原NO2至N2,放出的热量=
×1160kJ/mol=173.4kJ,故D正确;
故选:C.
B.等物质的量的甲烷分别参加反应①、②时,碳元素的化合价变化相同,所以反应转移的电子数相同,故B正确;
C.水蒸气液化放出热量,所以生成液态水放出热量多,所以得CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(l)△H=-akJ?mol-1,a>574,故C错误;
D.用标准状况下4.48L CH4还原NO2至N2,放出的热量=
| 4.48L |
| 22.4L/mol |
故选:C.
点评:本题考查了物质的量的有关计算、反应热的计算等知识点,题目比较简单.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
 (2010?祁阳县一模)一氧化碳、二氧化硫和氮的氧物是重要的化工原料,但也是大气的主要污染物,综合治理其污染是环境化学当前的重要研究内容之一.
(2010?祁阳县一模)一氧化碳、二氧化硫和氮的氧物是重要的化工原料,但也是大气的主要污染物,综合治理其污染是环境化学当前的重要研究内容之一.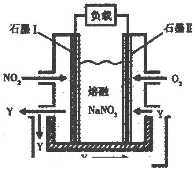
 汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一.
汽车内燃机工作时产生的高温会引起N2和O2发生反应生成NO气体,是导致汽车尾气中含有NO的原因之一.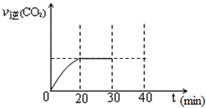 随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.