题目内容
10.美国航天局宣布,月球坑观测和传感卫星获得的撞月数据显示,月球上存在“数量可观的水”.下列有关说法正确的是( )| A. | 月球上的H2O分子中只含有非极性共价键 | |
| B. | H2O在化学反应中既可作氧化剂又可作还原剂 | |
| C. | 氢的三种同位素H、D、T与16O只能形成三种水分子 | |
| D. | 在标准状况下,1mol水的体积约是22.4L |
分析 A.H2O分子中只含有O-H键;
B.从化合价的角度分析;
C.根据水分子的构成进行分析,一个水分子中含有两个氢原子和一个氧原子,水分子所含有的氢原子可以是同一种氢原子,也可以是不同种氢原子;
D.标准状况下,水为液体.
解答 解:A.H2O分子中只含有O-H键,为极性键,故A错误;
B.水中H为+1价,为最高价态,O为-2价,为最低价态,水分解时,自身发生氧化还原反应,既是氧化剂也是还原剂,故B正确;
C.一个水分子中含有两个氢原子和一个氧原子,水分子所含有的氢原子可以是同一种氢原子,也可以是不同种氢原子,若是同一种氢原子,则能组成的水分子种类有3种,若是不同种氢原子,则由1H、2H、组成的水分子有1种,由2H、3H组成的水分子有1种,由1H、3H组成的水分子有1种,共有6种水分子,故C错误;
D.标准状况下,水为液体,1mol水的体积约是18mL,故D错误.
故选B.
点评 本题考查较为综合,涉及共价键、氧化还原反应、同位素以及物质的量的计算等知识,为高频考点,侧重于学生的分析能力的考查,难度不大,注意相关知识的学习和积累.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
18.已知标准状况下3.2g某气体的体积为1.12L,此气体的摩尔质量是( )
| A. | 32g/mol | B. | 64 | C. | 64g/mol | D. | 4g |
5.1.024×1023个水分子的物质的是( )
| A. | 0.3 mol | B. | 0.1 mol | C. | 0.2 mol | D. | 2 mol |
15.2.8gFe全部溶于一定浓度200mLHNO3溶液中,得到标准状况下气体1.12L,测得反应后溶液pH为1.若反应前后溶液体积变化忽略不计,则下列有关判断不正确的是( )
| A. | 反应后溶液中铁元素一定只以Fe3+形式存在 | |
| B. | 1.12L气体可能是NO、NO2的混合气体 | |
| C. | 反应后溶液中c(NO3-)=0.85mol/L | |
| D. | 反应后的溶液最多还能溶解1.82gFe |
20.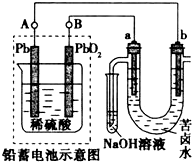 用铅蓄电池电解苦卤水(含C1-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是( )
用铅蓄电池电解苦卤水(含C1-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是( )
 用铅蓄电池电解苦卤水(含C1-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是( )
用铅蓄电池电解苦卤水(含C1-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极).下列说法中正确的是( )| A. | 铅蓄电池放电时,该电池两极质量均减小 | |
| B. | 铅蓄电池充电时,B极应与外电源负极相连 | |
| C. | 电解苦卤水时,a电极首先放电的是Cl-而不是Br-,因为Cl-的还原性强于Br- | |
| D. | 当b极产生0.01 mol 气体时,铅蓄电池中消耗0.02 molH2SO4 |

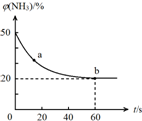 合理应用和处理氮的化合物,在生产生活中有重要意义.
合理应用和处理氮的化合物,在生产生活中有重要意义.