题目内容
18.已知标准状况下3.2g某气体的体积为1.12L,此气体的摩尔质量是( )| A. | 32g/mol | B. | 64 | C. | 64g/mol | D. | 4g |
分析 根据n=$\frac{V}{Vm}$计算1.12L该气体的物质的量,再根据M=$\frac{m}{n}$计算该气体的摩尔质量.
解答 解:1.4g气体在标准状况下的体积为1.12L,气体物质的量为n=$\frac{V}{Vm}$=$\frac{1.12L}{22.4L/mol}$=0.05mol,
故该气体的摩尔质量为:M=$\frac{m}{n}$=$\frac{3.2g}{0.05mol/L}$=64g/mol,
故选C.
点评 本题考查常用化学计量的有关计算,比较基础,注意对公式的理解与灵活运用,题目难度不大.

练习册系列答案
相关题目
9.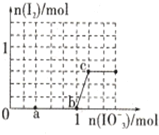 已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )
已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )
 已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )
已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )| A. | 还原性:HSO${\;}_{3}^{-}$>I-,氧化性:IO${\;}_{3}^{-}$>I2>SO${\;}_{4}^{2-}$ | |
| B. | a点处的氧化产物是SO${\;}_{4}^{2-}$,还原产物是I- | |
| C. | 当溶液中的I-为0.4mol时,加入的KIO3一定为0.4mol | |
| D. | 若向KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为:2IO${\;}_{3}^{-}$+5HSO${\;}_{3}^{-}$═I2+5SO${\;}_{4}^{2-}$+3H++H2O |
3.1gH2中含有原子数目( )
| A. | 0.5 mol | B. | 1 mol | C. | 1.5 mol | D. | 2 mol |
10.美国航天局宣布,月球坑观测和传感卫星获得的撞月数据显示,月球上存在“数量可观的水”.下列有关说法正确的是( )
| A. | 月球上的H2O分子中只含有非极性共价键 | |
| B. | H2O在化学反应中既可作氧化剂又可作还原剂 | |
| C. | 氢的三种同位素H、D、T与16O只能形成三种水分子 | |
| D. | 在标准状况下,1mol水的体积约是22.4L |
7.某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如图:

下列推断不合理的是( )

下列推断不合理的是( )
| A. | 往甲中通适量CO2有利于(NH4)2SO4生成 | |
| B. | 生成1 mol(NH4)2SO4至少消耗2 molNH3 | |
| C. | CO2可被循环利用 | |
| D. | NH3、CO2的通入顺序可以互换 |
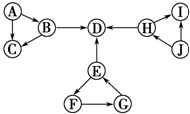 已知:①图中每个小三角形的三种物质中至少含有一种相同元素,H与I含有完全相同的元素.②A、J为固体单质,D为气体单质,其余物质为常见化合物.③B为淡黄色化合物,B与H反应能生成D.④E为常见金属氧化物.⑤F的溶液和H反应生成白色胶状沉淀G.
已知:①图中每个小三角形的三种物质中至少含有一种相同元素,H与I含有完全相同的元素.②A、J为固体单质,D为气体单质,其余物质为常见化合物.③B为淡黄色化合物,B与H反应能生成D.④E为常见金属氧化物.⑤F的溶液和H反应生成白色胶状沉淀G. .
.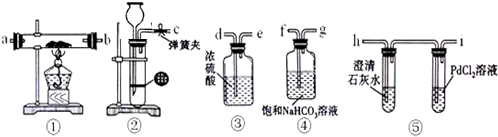
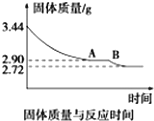 煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题:
煤是重要的能源,也是生产化工产品的重要原料.试用所学知识,解答下列问题: