题目内容
11.化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质.例如: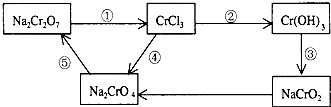
(1)在上述有编号的步骤中,需用还原剂的是①,需用氧化剂的是④ (填编号).
(2)完成并配平下列反应的化学方程式(用单线桥表示电子转移的方向、数目):
1Na2Cr2O7+6KI+14HCl--2CrCl3+2NaCl+6KCl+3I2+7H2O.
分析 (1)反应中①Cr元素化合价降低,②③Cr元素化合价不变,④Cr元素化合价升高,⑤Cr元素化合价不变;
(2)Cr元素化合价由+6价降低为+3价,I元素的化合价由-1价升高为0,该反应转移6e-,以此来解答.
解答 解:(1)反应中①Cr元素化合价降低,②③Cr元素化合价不变,④Cr元素化合价升高,⑤Cr元素化合价不变,则需用还原剂的是①,需用氧化剂的是④,
故答案为:①;④;
(2)Cr元素化合价由+6价降低为+3价,I元素的化合价由-1价升高为0,由电子、原子守恒可知,反应为Na2Cr2O7+6KI+14HCl=2CrCl3+2NaCl+6KCl+3I2+7H2O,该反应转移6e-,用单线桥表示电子转移的方向、数目为
故答案为:
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.一定温度下,对于两个可逆反应A(g)+2B(g )?2C(g)和A(s)+2B(g)?2C(g),都能说明两个反应都已达到平衡的是( )
| A. | 容器内总压强不再变化 | B. | 混合气体的密度不再变化 | ||
| C. | 混合气体的平均摩尔质量不再变化 | D. | 混合气体的总质量不再变化 |
19.下列说法正确的是( )
| A. | 已知氯化钴及其水合物会呈现不同颜色(如下),德国科学家发明了添加氯化钴的变色水泥,据此推测雨天变色水泥呈粉红色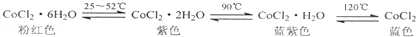 | |
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增大活化分子的百分数,从而使反应速率增大 | |
| C. | 2CO(g)═N2(g)+2CO2(g)在常温下能自发进行,则该反应的△H>0 | |
| D. | 对于乙酸与乙醇的酯化反应(△H<0),加入少量浓硫酸并加热,该反应的反应速率和平衡常数均增大 |
6.按下列实验方法操作,能达到要求的是( )
| A. | 用托盘天平称量25.20g氯化钠固体 | |
| B. | 苹果含有Fe2+,现榨苹果汁在空气中会由淡绿色变为棕黄色,若榨汁时加入具有还原性的维生素C,可防止该现象发生 | |
| C. | 某固体在加入稀盐酸产生了无色无味且能使澄清石灰水变浑浊的气体,证明该固体一定含有CO32- | |
| D. | 将氢氧化钠固体在容量瓶中溶解,配制一定物质的量浓度的NaOH溶液 |
16.在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO42-离子完全沉淀;如加入足量强碱并加热可得到c mol NH3,(已知NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O)则原溶液中的Al3+的物质的量浓度(mol•L-1)为( )
| A. | $\frac{2b-c}{2a}$ | B. | $\frac{2b-c}{a}$ | C. | $\frac{2b-c}{3a}$ | D. | $\frac{2b-c}{6a}$ |
1.下列说法正确的是( )
| A. | 绿色食品就是指颜色为绿色的食品 | B. | 白色污染是指白色的废弃物的污染 | ||
| C. | 食盐加碘是为了预防“大脖子”病 | D. | 有机食品是指含有有机物的食品 |

 .
.