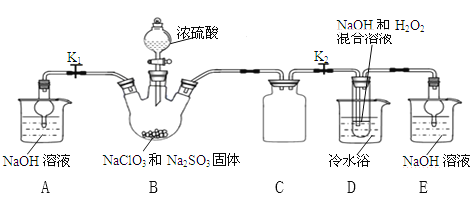
题目内容
【题目】下列说法不正确的是
A. 化学反应除了生成新物质外,还伴随着能量的变化
B. 对于ΔH>0的反应,反应物的总能量小于生成物的总能量
C. 放热反应都不需要加热就能发生
D. 吸热反应在一定条件(如常温、加热等)下也能发生
【答案】C
【解析】
试题A.化学反应的过程就是旧化学键断裂和新化学键形成的共存,所以除了生成新物质外,还伴随着能量的变化,正确;B.对于ΔH>0的反应,是吸热反应,即反应物的能量小于生成物的能量,正确;C.任何反应发生都要断裂化学键形成单个的原子,所以放热反应也需要吸收一定的能量才能发生,错误;D.吸热反应在一定条件(如常温、加热等)下当获得足够的能量时也可以发生,正确。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
【题目】(1)已知反应2H2 + O2 ![]() 2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量 __________kJ
2H2O为放热反应,破坏1mol的化学键消耗的能量称为化学键的键能。有关物质中化学键的键能如下表,则生成1mol水可以放出热量 __________kJ
化学键 | H—H | O=O | H—O |
键能kJ/mol | 436 | 496 | 463 |
(2)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如下图所示,A、B两个电极均由多孔的碳块组成。

①B作_____极材料(填“正”或“负”),电解质溶液中SO42- 移向_____极(填“A”或“B”)。
②写出A极的电极反应式_______,一段时间后,溶液的PH______(填“升高”“降低”“不变”),
③如果将上述装置中通入的H2改成CH4气体,也可以组成一个原电池装置,当有标准状况下11.2L CH4完全反应时,导线中通过的电子的数目__________。