题目内容
【题目】盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现据“三大酸”与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解,该反应的离子方程式为_。
(2)在一定体积的18mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol,则浓硫酸的实际体积__(填“大于”“等于”或“小于”)100mL。若使剩余的铜片继续溶解,可向其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为__。
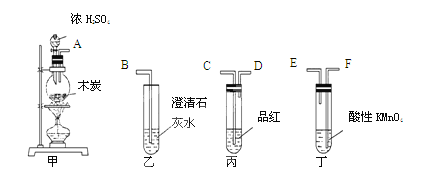
(3)根据如图操作及现象推断酸X为__(填序号)。
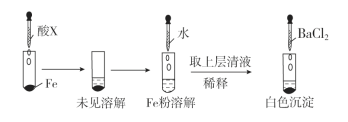
A.浓盐酸 B.浓硫酸 C.浓硝酸
【答案】Cu+H2O2+2H+=Cu2++2H2O 大于 3Cu+8H++2NO![]() =3Cu2++2NO↑+4H2O B
=3Cu2++2NO↑+4H2O B
【解析】
(1)双氧水具有氧化性,在酸性环境下能将金属铜氧化溶解铜;
(2)铜只能和浓硫酸反应,同稀硫酸不反应,若使剩余的铜片继续溶解,可向其中加入硝酸盐,因溶液中有H+,再加入硝酸盐引入NO3-,相当于存在了硝酸,硝酸能将铜溶解;
(3)因浓硫酸和浓硝酸在常温下能使金属铁发生钝化,因最终向铁粉溶液中加入BaCl2会产生白色沉淀,故该溶液中含有SO42-,据此分析解答。
(1)双氧水具有氧化性,在酸性环境下能将金属铜氧化,方程式为:Cu+H2O2+2HCl=2H2O+CuCl2,离子反应为:Cu+H2O2+2H+=Cu2++2H2O;
(2)铜只能和浓硫酸反应,同稀硫酸不反应,Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,随着铜和浓硫酸的反应的进行,酸的浓度越来越小,不再产生二氧化硫,浓硫酸在反应中既显氧化性又显酸性,当被还原的硫酸是0.9mol,则18molL-1的浓硫酸的实际体积要大于100mL;若使剩余的铜片继续溶解,可向其中加入硝酸盐,因溶液中有H+,再加入硝酸盐引入NO3-,相当于存在了硝酸,硝酸能将铜溶解,反应实质为:3Cu+8H++2NO
CuSO4+SO2↑+2H2O,随着铜和浓硫酸的反应的进行,酸的浓度越来越小,不再产生二氧化硫,浓硫酸在反应中既显氧化性又显酸性,当被还原的硫酸是0.9mol,则18molL-1的浓硫酸的实际体积要大于100mL;若使剩余的铜片继续溶解,可向其中加入硝酸盐,因溶液中有H+,再加入硝酸盐引入NO3-,相当于存在了硝酸,硝酸能将铜溶解,反应实质为:3Cu+8H++2NO![]() =3Cu2++2NO↑+4H2O;
=3Cu2++2NO↑+4H2O;
(3)因浓硫酸在常温下能使金属铁发生钝化,而稀硫酸能与铁发生反应,因最终向铁粉溶液中加入BaCl2会产生白色沉淀,故该溶液中含有SO42-,所以根据现象,可推断酸X为浓硫酸,答案选B。

【题目】已知:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O.
某化学小组根据上述反应原理进行下列实验:
I.测定H2C2O4溶液的物质的量浓度
实验步骤如下:
①取待测H2C2O4溶液25.00mL放入锥形瓶中,再加入适量的稀硫酸;
②用0.1mol/LKMnO4溶液滴定至终点,记录数据;
③重复滴定2次,平均消耗KMnO4溶液20.00mL。
请回答:
(1)滴定时,将KMnO4溶液装在______(填“酸式”或“碱式”)滴定管中。
(2)若在步骤①操作之前,先用待测H2C2O4溶液润洗锥形瓶,则测得H2C2O4溶液的浓度会______(填“偏大”“偏小”或“无影响”)。
(3)步骤②中到达滴定终点时的现象为_______________________________。
(4)计算H2C2O4溶液的物质的量浓度为__________mol/L。
II.探究反应物浓度对化学反应速率的影响设计如下实验方案(实验温度均为25℃):
实验序号 | 体积V/mL | |||
0.1molL-1KMnO4溶液 | 0.11molL-1H2C2O4溶液 | 0.11molL-1H2SO4溶液 | H2O | |
① | 2.0 | 5.0 | 6.0 | 7.0 |
② | 2.0 | 8.0 | 6.0 | V1 |
③ | 2.0 | V2 | 6.0 | 2.0 |
请回答:
(5)表中v1=______。
(6)实验中需要测量的数据是______________________________。
(7)实验中______(填“能”或“不能”)用0.2mol/L盐酸代替0.1mol/LH2SO4溶液,理由是_________。