题目内容
【题目】某小组用如图装置进行实验,下列说法正确的是( ) 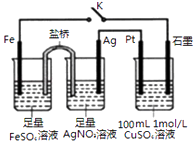
A.盐桥中的电解质可以用KC1
B.闭合K,石墨电极上只生成铜
C.当有0.1mol Fe溶解时,流经电解液的电子个数为1.204×1023
D.导线中流过0.3mol电子时,加入11.1gCu2(OH)2CO3 , CuSO4溶液可恢复原组成
【答案】D
【解析】 解:A.由于KCl能和AgNO3产生沉淀,因此盐桥中的电解质不能用KCl,故A错误;
B.闭合K,与铁相连的石墨为阴极,发生还原反应首先Cu2++2e﹣═Cu,析出Cu,后发生2H++2e﹣═H2 , 放出氢气,故B错误;
C.0.1mol铁失去0.2mol电子,但电子不能通过溶液传递,而是经过导线,故C错误;
D.CuSO4溶液中n(Cu2+)=0.1mol,完全消耗时转移电子数为0.2mol,导线中流过03mol e﹣说明水也参与了电解,电解CuSO4的总反应2Cu2++2H2O ![]() 2Cu+O2↑+4H+ , 溶液中减少的是2Cu和O2(相当于2CuO),需要补充0.1molCuO,电解水的总反应2H2O
2Cu+O2↑+4H+ , 溶液中减少的是2Cu和O2(相当于2CuO),需要补充0.1molCuO,电解水的总反应2H2O ![]() 2H2↑+O2↑,转移电子数为0.1mol,因此消耗0.05mol的H2O,Cu2(OH)2CO3可写为2CuOH2OCO2 , 所以加入0.05mol×222g/mol=11.1g Cu2(OH)2CO3 , CuSO4溶液可恢复原组成,故D正确;
2H2↑+O2↑,转移电子数为0.1mol,因此消耗0.05mol的H2O,Cu2(OH)2CO3可写为2CuOH2OCO2 , 所以加入0.05mol×222g/mol=11.1g Cu2(OH)2CO3 , CuSO4溶液可恢复原组成,故D正确;
故选D.

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案【题目】某同学按下列步骤配制100mL0.200molL﹣1Na2CO3溶液,请回答有关问题.
实验步骤 | 有关问题 |
(1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为 . |
(2)称量Na2CO3固体 | 称量过程中应用到的主要仪器是 . |
(3)将Na2CO3加入100mL烧杯中,加入适量蒸馏水 | 为了加快溶解速率,常采取的措施是 . |
(4)将烧杯中的溶液转移至仪器A(已检查不漏水)中 | ①在转移Na2CO3溶液前应将溶液 ; |
(5)向仪器A中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是 . |
(6)摇匀、装瓶,操作B,最后清洁、整理 | 操作B是 . |
讨论按上述步骤配制的Na2CO3溶液的浓度 (选填“是”或“不是”)0.200molL﹣1 . 理由是 .
