题目内容
下列有关溶液中微粒浓度关系的叙述正确的是( )
分析:A.等浓度的(NH4)2SO4溶液,NH4HSO4溶液和NH4Cl溶液,由水解可知c(NH4+)关系,反之,c(NH4+)相等可判断盐溶液的浓度关系;
B.pH相等,则两溶液中c(H+)、c(OH-)相等,结合溶液的电荷守恒判断;
C.根据电荷守恒和物料守恒判断;
D.从物料守恒的角度判断.
B.pH相等,则两溶液中c(H+)、c(OH-)相等,结合溶液的电荷守恒判断;
C.根据电荷守恒和物料守恒判断;
D.从物料守恒的角度判断.
解答:解:A.等浓度的(NH4)2SO4溶液,NH4HSO4溶液和NH4Cl溶液,由水解可知c(NH4+)的关系为c[(NH4)2SO4]>c[NH4HSO4]>c(NH4Cl),则c(NH4+)相等时,三种盐溶液的浓度关系为c[(NH4)2SO4]<c[NH4HSO4]<c(NH4Cl),故A错误;
B.pH相等,则两溶液中c(H+)、c(OH-)相等,NaF溶液中存在c(Na+)+c(H+)=c(F-)+c(OH-),CH3COOK溶液中存在c(K+)+c(H+)=c(CH3COO-)+c(OH-),则有[c(Na+)-c(F-)]=[c(K+)-c(CH3COO-)]=[c(OH-)-c(H+)],故B错误;
C.等物质的量浓度Na2CO3溶液和NaHCO3溶液等体积混合中存在电荷守恒:2c(CO32-)+c(OH-)+c(HCO3-)=c(Na+)+c(H+),根据物料守恒可知存在2c(Na+)=3c(HCO3-)+3c(H2CO3)+3c(CO32-),二者联式可得c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3),故C正确;
D.溶有等物质的量NaClO、NaHCO3的溶液中存在物料守恒,应为c(HClO)+c(C1O-)=c(HCO3-)+c(H2CO3)+c(CO32-)=
c(Na+),故D错误.
故选C.
B.pH相等,则两溶液中c(H+)、c(OH-)相等,NaF溶液中存在c(Na+)+c(H+)=c(F-)+c(OH-),CH3COOK溶液中存在c(K+)+c(H+)=c(CH3COO-)+c(OH-),则有[c(Na+)-c(F-)]=[c(K+)-c(CH3COO-)]=[c(OH-)-c(H+)],故B错误;
C.等物质的量浓度Na2CO3溶液和NaHCO3溶液等体积混合中存在电荷守恒:2c(CO32-)+c(OH-)+c(HCO3-)=c(Na+)+c(H+),根据物料守恒可知存在2c(Na+)=3c(HCO3-)+3c(H2CO3)+3c(CO32-),二者联式可得c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3),故C正确;
D.溶有等物质的量NaClO、NaHCO3的溶液中存在物料守恒,应为c(HClO)+c(C1O-)=c(HCO3-)+c(H2CO3)+c(CO32-)=
| 1 |
| 2 |
故选C.
点评:本题综合考查溶液离子浓度的大小比较,侧重于学生分析能力和计算能力的考查,题目难度较大,本题注意溶液的电荷守恒、物料守恒的综合应用,易错点为C、D,注意把握.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
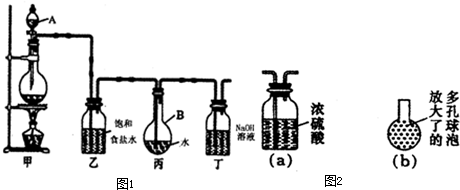
 H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。
H++F-。25℃下,向20mL0.2mol?L-1的氢氟酸中滴加0.2mol?L-1的NaOH溶液时,溶液的pH变化如图所示。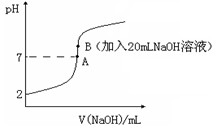
 )和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力,
)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力, 。
。 约为___ _%。
约为___ _%。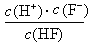 = Ka(HF)
= Ka(HF) H++F-。25℃下,向20mL0.2mol•L-1的氢氟酸中滴加0.2mol•L-1的NaOH溶液时,溶液的pH变化如图所示。
H++F-。25℃下,向20mL0.2mol•L-1的氢氟酸中滴加0.2mol•L-1的NaOH溶液时,溶液的pH变化如图所示。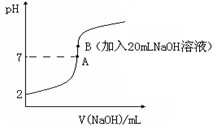
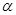 )和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力,
)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力, 。
。 约为___
_%。
约为___
_%。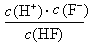 = Ka(HF)
= Ka(HF)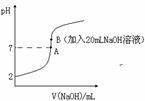 已知:电离度(
已知:电离度(