题目内容
10.下列离子方程式正确的是( )| A. | 向氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | |
| C. | Fe(NO3)3 溶液中加入过量HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | 碳酸氢铵溶液中加入足量NaOH溶液:NH4++HCO3-+2OH-═CO32-+NH3•H2O+H2O |
分析 A.一水合氨为弱碱,二者反应生成氢氧化铝沉淀;
B.苯酚的酸性大于碳酸氢根离子,二者反应生成苯酚和碳酸氢根离子;
C.碘化钾过量,硝酸根离子在酸性条件下具有强氧化性,铁离子和硝酸根离子都参与反应;
D.强氧化钠足量,铵根离子和碳酸氢根离子都完全反应.
解答 解:A.向氯化铝溶液中加入过量的氨水,反应生成氢氧化铝沉淀和氯化铵,正确的离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故A错误;
B.苯酚钠溶液中通入少量CO2,二者反应生成碳酸氢根离子和苯酚,正确的离子方程式为:CO2+H2O+C6H5O-→C6H5OH+HCO3-,故B错误;
C.Fe(NO3)3 溶液中加入过量HI溶液,反应生成碘化亚铁、碘单质、NO气体和水,正确的离子方程式为:10I-+3NO3-+Fe3++12H+═5I2+3NO↑+Fe2++6H2O,故C错误;
D.碳酸氢铵溶液中加入足量NaOH溶液,反应生成碳酸钠、一水合氨和水,反应的离子方程式为:NH4++HCO3-+2OH-═CO32-+NH3•H2O+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,该题是高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
11.向下列各组物质反应后的溶液中,滴入KSCN溶液,一定显红色的是( )
| A. | Fe和稀硫酸 | B. | Fe和FeCl3溶液 | C. | FeO和稀硫酸 | D. | Fe2O3和稀盐酸 |
1.下列各组离子能在溶液中大量共存的是( )
| A. | HCO3-、Na+、OH-、K+ | B. | Cl-、NO3-、Fe2+、H+ | ||
| C. | Ba2+、OH-、Cl-、Na+ | D. | NH4+、Na+、NO3-、OH- |
18.如表为元素周期表短周期的一部分.下列有关A、B、C、D、E 五种元素的叙述中正确的是( )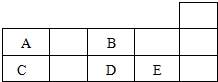

| A. | 对应阴离子的还原性:E>D | B. | 原子半径:C>B | ||
| C. | 对应氧化物的水化物的酸性:E>D | D. | A的非金属性弱于D |
5.有关如图装置中的叙述不正确的是( )
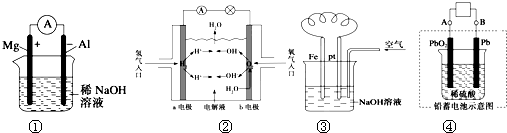

| A. | 图①铝片发生的电极反应式是:Al+4OH--3e═AlO2-+2H2O | |
| B. | 图②b电极的电极反应为:4OH--4e-═2H2O+O2↑ | |
| C. | 图③溶液中发生了变化:4Fe(OH)2+O2+2H2O═4Fe(OH)3 | |
| D. | 图④充电时:阳极反应是PbSO4+2H2O-2e-═PbO2+SO42-+4H+ |
15.下列有机物命名不正确的是( )
| A. | 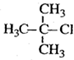 2-甲基-2-氯丙烷 2-甲基-2-氯丙烷 | B. | 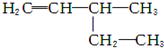 3-乙基-1-丁烯 3-乙基-1-丁烯 | ||
| C. | 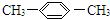 1,4-二甲苯 1,4-二甲苯 | D. | 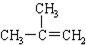 2-甲基丙烯 2-甲基丙烯 |
19.下列物质不属于天然高分子材料的是( )
| A. | 棉花 | B. | 塑料 | C. | 蚕丝 | D. | 羊毛 |
20.芬兰Enfucell公司制造出一种纸质电池(如图所示),避免了传统电池所带来的金属及碱性化合物的泄漏问题,因而可作为一般的家庭废物加以处理.这种被称之为“软电池”的纸质电池,采用一个薄层纸片作为传导体,在其一边镀锌,而在其另一边镀二氧化锰,在纸内的离子“流过”水和氧化锌组成的电解质溶液.电池总反应为:Zn+2MnO2+H2O═2MnO(OH)+ZnO.下列说法正确的是( )

| A. | 该电池的正极为锌 | |
| B. | 该电池反应中二氧化锰起催化剂作用 | |
| C. | 当0.1molZn完全溶解时,流经电解质溶液的电子个数为1.204×1023 | |
| D. | 电池正极反应式为:2MnO2+2e-+2H2O═2MnO(OH)+2OH- |
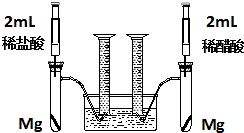 某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图:
某化学小组为比较盐酸和醋酸的酸性,设计了如下实验方案.装置如图: