题目内容
5.有关如图装置中的叙述不正确的是( )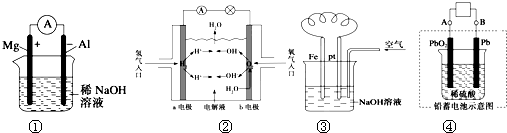
| A. | 图①铝片发生的电极反应式是:Al+4OH--3e═AlO2-+2H2O | |
| B. | 图②b电极的电极反应为:4OH--4e-═2H2O+O2↑ | |
| C. | 图③溶液中发生了变化:4Fe(OH)2+O2+2H2O═4Fe(OH)3 | |
| D. | 图④充电时:阳极反应是PbSO4+2H2O-2e-═PbO2+SO42-+4H+ |
分析 A.该装置中Al作负极、Mg作正极,负极上Al失电子和氢氧根离子反应生成偏铝酸根离子;
B.该装置中通入氢气的电极是负极、通入氧气的电极是正极,所以b是正极,正极上氧气得电子和氢离子反应生成水;
C.该装置发生吸氧腐蚀,Fe作负极、Pt作正极,Fe失电子生成亚铁离子,正极上氧气得电子和水反应生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧气氧化生成氢氧化铁;
D.充电时,阳极上硫酸铅失电子生成二氧化铅和硫酸.
解答 解:A.该装置中Al作负极、Mg作正极,负极上Al失电子和氢氧根离子反应生成偏铝酸根离子,铝片发生的电极反应式是:Al+4OH--3e═AlO2-+2H2O,故A正确;
B.该装置中通入氢气的电极是负极、通入氧气的电极是正极,所以b是正极,正极上氧气得电子和氢离子反应生成水,b电极的电极反应为:2H2O+O2+4e-═4OH-,故B错误;
C.该装置发生吸氧腐蚀,Fe作负极、Pt作正极,Fe失电子生成亚铁离子,正极上氧气得电子和水反应生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧气氧化生成氢氧化铁,所以图③溶液中发生了变化:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故C正确;
D.充电时,阳极上硫酸铅失电子生成二氧化铅和硫酸,充电时:阳极反应是PbSO4+2H2O-2e-═PbO2+SO42-+4H+,故D正确;
故选B.
点评 本题考查电极反应式的书写,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写,题目难度中等.

练习册系列答案
相关题目
6.实验室可用右图所示的装置干燥、收集某气体R,则R可能是( )
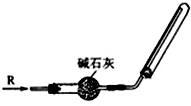

| A. | NH3 | B. | SO2 | C. | HCl | D. | O2 |
7.已知常温下在溶液中可以发生如下两个离子反应:
Ce4++Fe2+→Fe3++Ce3+
Sn2++2Fe3+→2Fe2++Sn4+,
由此可以确定Ce4+、Ce3+、Fe3+三种离子的氧化性由强到弱的顺序( )
Ce4++Fe2+→Fe3++Ce3+
Sn2++2Fe3+→2Fe2++Sn4+,
由此可以确定Ce4+、Ce3+、Fe3+三种离子的氧化性由强到弱的顺序( )
| A. | Ce4+、Ce3+、Fe3+ | B. | Ce4+、Fe3+、Ce3+ | C. | Fe3+、Ce4+、Ce3+ | D. | Ce3+、Ce4+、Fe3+ |
13.下列化学用语正确的是( )
| A. | Na2S2中硫元素的化合价为-2 | B. | NH4Cl的电子式: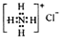 | ||
| C. | S2-的结构示意图: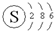 | D. | COCl2的电子式: |
20.我国报道的高温超导体中,铊是组成成分之一.已知铊和铝的性质相似,下列关于铊的判断正确的是( )
| A. | 氢氧化铊是两性氢氧化物 | |
| B. | 铊是两性金属 | |
| C. | 铊是金属 | |
| D. | 氧化铊既能与盐酸反应,又能与氢氧化钠溶液反应 |
10.下列离子方程式正确的是( )
| A. | 向氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| B. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- | |
| C. | Fe(NO3)3 溶液中加入过量HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | 碳酸氢铵溶液中加入足量NaOH溶液:NH4++HCO3-+2OH-═CO32-+NH3•H2O+H2O |
17.实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表.
操作如下:
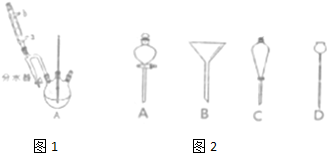
①在50mL三颈烧瓶中,加入18.5mL正丁醇和13.4mL冰醋酸,3~4滴浓硫酸,投入沸石.安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管.(如图1)
②将分水器分出的酯层和反应液一起倒入分液漏斗中,水洗,10%Na2CO3洗涤,再水洗,最后转移至锥形瓶,干燥.
③将干燥后的乙酸正丁酯滤入烧瓶中,常压蒸馏,收集馏分,得15.1g乙酸正丁酯.
请回答有关问题:
(1)冷水应该从冷凝管a(填a或b)端管口通入.
(2)仪器A中发生反应的化学方程式为CH3COOH+CH3CH2CH2CH2OH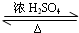 CH3COOCH2CH2CH2CH3+H2O.
CH3COOCH2CH2CH2CH3+H2O.
(3)步骤①“不断分离除去反应生成的水”该操作的目的是:使用分水器分离出水,使平衡正向移动,提高反应产率.
(4)步骤②中,用10%Na2C03溶液洗涤有机层,该步操作的目的是除去产品中含有的乙酸等杂质.
(5)进行分液操作时,使用的漏斗是C(填选项).(如图2)
(6)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏高(填“高”或者“低”)原因是会收集到少量未反应的冰醋酸和正丁醇.
| 化合物 | 相对分子质量 | 密度/g/cm3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |

操作如下:
①在50mL三颈烧瓶中,加入18.5mL正丁醇和13.4mL冰醋酸,3~4滴浓硫酸,投入沸石.安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管.(如图1)
②将分水器分出的酯层和反应液一起倒入分液漏斗中,水洗,10%Na2CO3洗涤,再水洗,最后转移至锥形瓶,干燥.
③将干燥后的乙酸正丁酯滤入烧瓶中,常压蒸馏,收集馏分,得15.1g乙酸正丁酯.
请回答有关问题:
(1)冷水应该从冷凝管a(填a或b)端管口通入.
(2)仪器A中发生反应的化学方程式为CH3COOH+CH3CH2CH2CH2OH
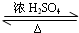 CH3COOCH2CH2CH2CH3+H2O.
CH3COOCH2CH2CH2CH3+H2O.(3)步骤①“不断分离除去反应生成的水”该操作的目的是:使用分水器分离出水,使平衡正向移动,提高反应产率.
(4)步骤②中,用10%Na2C03溶液洗涤有机层,该步操作的目的是除去产品中含有的乙酸等杂质.
(5)进行分液操作时,使用的漏斗是C(填选项).(如图2)
(6)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏高(填“高”或者“低”)原因是会收集到少量未反应的冰醋酸和正丁醇.
14.在同温同压下,下列各组热化学方程式中,△H1<△H2的是( )
| A. | 2H2(气)+O2(气)═2H2O(气)△H1 2H2(气)+O2(气)═2H2O(液)△H2 | |
| B. | S(气)+O2(气)═SO2(气)△H1 S(固)+O2(气)═SO2(气)△H2 | |
| C. | C(固)+$\frac{1}{2}$O2 (气)═CO(气)△H1 C(固)+O2 (气)═CO2(气)△H2 | |
| D. | H2(气)+Cl2(气)═2HCl(气)△H1 $\frac{1}{2}$H2(气)+$\frac{1}{2}$Cl2(气)=HCl(气)△H 2 |
15.如图装置所示,负极上发生的反应为( )
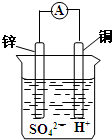

| A. | Zn2++2e-═Zn | B. | Zn-2e-═Zn2+ | C. | Cu-2e-═Cu2+ | D. | Cu2++2e-═Cu |