题目内容
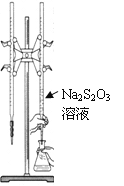
【题目】亚硝酸钠(NaNO2)是工业盐的主要成分,在漂白、电镀等方面应用广泛。已知:室温下,2NO+Na2O2====2NaNO2,以木炭、浓硝酸、Na2O2为主要原料制备亚硝酸钠的装置如图所示。(加热装置及部分夹持装置已略去)

回答下列问题:
(1)A装置中反应的化学方程式为__________________________________________。
(2)B装置的作用是_________________________________________________。
(3)充分反应后,C中生成的固体除NaNO2外,还可能生成_________(填化学式),为避免杂质的生成,应在B、C之间加一个为_________装置,该装置和所盛放试剂的名称分别是____________。
(4)检查装置气密性并装入药品后,以下实验操作步骤正确的顺序为_________( (填标号)。
a.打开弹簧夹,向装置中通入N2 b.点燃酒精灯
c.向三颈烧瓶中滴加浓硝酸 d.熄灭酒精灯
e.关闭分液漏斗旋塞 f.停止通入N2
(5)D装置用于尾气处理,写出D中反应的离子方程式:________________________。
【答案】C+4HNO3(浓)![]() CO2+4NO2+2H2O 将NO2转化为NO Na2CO3、NaOH 干燥管 碱石灰 acebdf
CO2+4NO2+2H2O 将NO2转化为NO Na2CO3、NaOH 干燥管 碱石灰 acebdf ![]()
【解析】
试题(1)A中浓硝酸与木炭在加热条件下发生氧化还原反应生成二氧化碳、二氧化氮、水;(2)本实验的目的是2NO+Na2O2====2NaNO2,所以B装置中把NO2转化为NO;(3)从B装置出来的气体含有CO2、H2O,C中Na2O2与CO2、H2O反应生成Na2CO3、NaOH;为避免杂质的生成,用碱石灰吸收 CO2、H2O;(4)NO能与氧气反应生成NO2,先用氮气排出装置中的空气,加入硝酸后加热,反应结束后停止加热,用氮气把装置中的NO全部排入D装置吸收。(5)D中NO被高锰酸钾氧化为硝酸根离子;
解析:(1)浓硝酸与木炭在加热条件下发生氧化还原反应的化学方程式C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O。
CO2↑+4NO2↑+2H2O。
(2)A中生成的二氧化氮进入B中并与水反应,生成了硝酸和 NO,硝酸和铜反应生成NO, D装置的作用是将NO2转化为NO。
(3)从B装置出来的气体含有CO2、H2O,C中Na2O2与CO2、H2O反应生成Na2CO3、NaOH,为避免产生这些副产物应在B、C装置间增加干燥管,药品名称是碱石灰。
(4)NO与氧气反应生成NO2,先用氮气排出装置中的空气,加入硝酸后加热,反应结束后停止加热,用氮气把装置中的NO全部排入D装置吸收。所以实验操作步骤正确的顺序为acebdf;
(5)D中反应的离子方程式![]() 。
。