题目内容
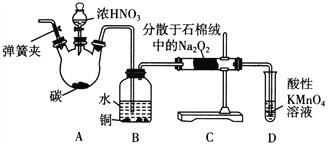
【题目】在如图所示的物质转化关系中,A、H为常见的金属单质,其中A为紫红色金属;D、F为气体,其中F为黄绿色气体;B、G为两种常见的酸;由J生成I的反应是电子工业常用的反应。(部分生成物和反应条件未列出)

请回答下列问题:
(1)F的电子式为 ____________ 。
(2)G的化学式为 ____________。
(3)写出反应①的化学方程式:______________________________________________
(4)写出由J生成I的离子方程式:______________________________________。
【答案】 HCl Cu+2H2SO4(浓)
HCl Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O 2Fe3++Cu=2Fe2++Cu2+
CuSO4+SO2↑+2H2O 2Fe3++Cu=2Fe2++Cu2+
【解析】
A、H为常见的金属单质,其中A为紫红色金属,则A为Cu;F为黄绿色气体,则F为氯气;D与氯气反应生成B、G为两种常见的酸,且B能够与Cu反应生成C、D、E,则B为硫酸、D为二氧化硫、G为盐酸;金属H与盐酸反应生成I,I能够与氯气反应生成J,J能够与Cu反应生成I,则H为Fe,I为氯化亚铁、J为氯化铁,Cu与氯化铁的反应是电子工业常用于制电路板的反应。
(1)F为氯气,氯气是双原子分子,电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(2)二氧化硫与氯气在溶液中反应生成硫酸和盐酸,硫酸能够与Cu反应,则B为硫酸,G为盐酸,故答案为:HCl;
(3)铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水,反应的方程式为Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(4)I为氯化亚铁、J为氯化铁,铁离子与铜反应生成氯化亚铁和氯化铜,反应的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故答案为:2Fe3++Cu═2Fe2++Cu2+。

 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案【题目】设计实验,对下列物质所含官能团进行检验。
(1)为了证明溴乙烷中存在溴原子,某同学设计如下实验:
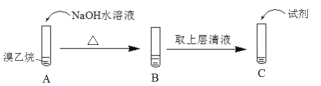
① 将试管C中加入的试剂及相应的实验现象补充完整:_______。
② 溴乙烷在NaOH水溶液中反应的化学方程式是______。
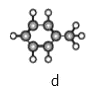
(2)用化学方法检验![]() 含有的官能团。
含有的官能团。
① 完成下表:
官能团 | 检验试剂 | 实验现象 | 化学方程式 |
—OH | FeCl3溶液 | 溶液呈紫色 |
|
—COOH | _______ | 有无色气泡产生 | _______ |
② 不能用溴水检验是否含有碳碳双键,简述理由:_______。