题目内容
下列有关化学用语正确的是
A.Na2S的电子式: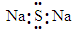 |
| B.铯—137:137Cs |
C.O2―的结构示意图: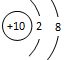 |
D.乙烯分子的球棍模型: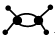 |
D
解析试题分析:Na2S是活泼金属与非金属元素形成的离子化合物,不是共价化合物,它只含离子键,不含共价键,故A错误;质量数位于核素符号的左上角,质子数位于核素符号的左下角,铯—137表示质量数为137的铯原子,符号为137Cs 或137 55Cs,故B错误;O2―的核电荷数与氧原子相同,因此结构示意图的圆圈内应为+8,而不是+10,故C错误;乙烯的分子式为C2H4,结构简式为H2C=CH2或CH2=CH2,故D正确。
考点:考查电子式、核素符号(A ZX)、简单离子结构示意图、常见有机物的球棍模型的识别与判断,涉及离子键和共价键、质量数与质子数、原子与离子、分子式与结构简式等知识。

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
下列化学用语正确的是 ( )
| A.HCN分子的结构式:H-C≡N |
| B.乙烯的结构简式:CH2CH2 |
C.F-离子结构示意图: |
D.二氧化碳的电子式: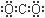 |
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1 mol,下列说法一定正确的是
| A.b="2" |
| B.反应中转移的电子数一定为2NA |
| C.容器中一定没有残余的CO2和水蒸气 |
| D.a:b≥1 |
设NA为阿伏加德罗常数,下列说法正确的是
| A.标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
| B.1 mol硫酸钾中阴离子所带电荷数为NA |
| C.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D.常温下,0.1mol/L的NH4NO3溶液中氮原子数为0.2NA |
设阿伏加德罗常数(NA)的数值为nA,下列说法正确的是(相对原子质量:H-1、O-16)
| A.11.2LNH3所含分子数为0.5nA |
| B.1molCl2与足量Fe反应,转移的电子数为3nA |
| C.100mL1mol/LFeCl3溶液中含Fe3+微粒的数目是0.1nA |
| D.常温下,34gH2O2中H-O键数目为2nA |
若NA表示阿伏加德罗常数,下列说法正确的是
| A.标准状况下,2.24LCl2与过量的稀NaOH 溶液反应,转移电子总数为0.2NA |
| B.1 mol·L-1 CaCl2溶液含有2NA个Cl- |
| C.在标准状况下,22.4L空气中约有NA个气体分子 |
| D.25℃时,l L pH=13的Ba(OH)2溶液中含 Ba2+的数目为0.1NA |
设nA为阿伏加德罗常数的数值,下列说法正确的是
| A.标准状况下,11.2L的H2O中含有的原子数为1.5nA |
| B.0.1mol·L-1 的(NH4)2SO4溶液中,所含NH4+数小于0.2nA |
| C.常温常压下,16g的O2和O3混合气体中,含有的电子数为8 nA |
| D.质量相同的N2和CO中,含有的原子数均为2nA |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1L0.5mol·L-1 的(NH4)2SO4溶液中含NH4+数为NA |
| B.常温常压下,1molCH4中含有4NA个C-H键 |
| C.常温常压下,48g O3含有原子数为2NA(相对原子质量:O 16) |
| D.标准状况下,22.4LC6H6(苯)的分子数目为NA |
将一质量分数为ω的KOH溶液蒸发掉m g水后,质量分数恰好变为3ω,体积为VL(溶液中无晶体析出),则浓缩后溶液的物质的量浓度为( )
A. mol·L-1 mol·L-1 | B. mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 | D. mol·L-1 mol·L-1 |