题目内容
17.下列有机物分子中,所有原子一定在同一平面内的( )| A. | 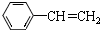 | B. |  | C. | 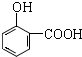 | D. | HC≡CCH=CHC≡CH |
分析 在常见的有机化合物中甲烷是正四面体结构,乙烯和苯、甲醛是平面型结构,其它有机物可在此基础上进行判断.
解答 解:A.乙烯和苯是平面型结构,但两个平面不一定在同一平面上,故A错误;
B.羟基上的氢与苯环不在同一平面上,故B错误;
C.羧基上的氢与苯环不在同一平面上,故C错误;
D.乙烯是平面型结构,乙炔是直线型分子,一定在同一平面上,故D正确.
故选D.
点评 本题考查有机物的空间结构,题目难度不大,注意把握甲烷、乙烯和苯的结构特点.

练习册系列答案
相关题目
7.工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g).已知在25℃时:
C(石墨)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol
C(石墨)+O2(g)═CO2(g)△H=-394kJ/mol
则25℃时1mol CO与水蒸气作用转化为氢气和二氧化碳反应△H为( )
C(石墨)+$\frac{1}{2}$O2(g)═CO(g)△H=-111kJ/mol
H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ/mol
C(石墨)+O2(g)═CO2(g)△H=-394kJ/mol
则25℃时1mol CO与水蒸气作用转化为氢气和二氧化碳反应△H为( )
| A. | +41.kJ/mol | B. | -41kJ/mol | C. | 283kJ/mol | D. | -131kJ/mol |
5.既含有极性共价键又含有非极性共价键的物质是( )
| A. | 甲烷 | B. | 乙烷 | C. | 水 | D. | 氧气. |
2.如图是某含C、H、O、N四种元素的有机分子的球棍模型.下列有关该有机物的说法错误的是( )
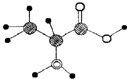

| A. | 其结构简式为:CH3CH(NH2)COOH | |
| B. | 该有机物含有两种官能团 | |
| C. | 该有机物的核磁共振氢谱显示7个吸收峰 | |
| D. | 该有机物能跟NaHCO3溶液反应产生CO2气体 |
9.下列不能达到预期目的相关实验是( )
| 相关实验 | 预期目的 | |
| A | 向酒精和醋酸的混合液中加入金属钠 | 确定酒精中混有醋酸 |
| B | 用核磁共振氢谱的方法 | 鉴别1-溴丙烷和2-溴丙烷 |
| C | 在蔗糖中加入稀H2SO4,水浴加热,用NaOH溶液中和后,再加入新制的氢氧化铜并加热 | 探究蔗糖水解产物是否具有还原性 |
| D | 将溴乙烷与NaOH溶液共热一段时间后,滴加AgNO3溶液 | 检验水解产物中的溴离子 |
| A. | A | B. | B | C. | C | D. | D |
6.在刚性密闭容器中加入P、Q发生下列反应,P(g)+2Q(g)?2S(g)+R(s)下列说法可以说明反应已达平衡的是( )
| A. | 反应容器中压强不随时间变化而变化 | |
| B. | 反应容器中P、Q、R、S四者共存 | |
| C. | P和R的生成速率相等 | |
| D. | 反应容器中物质的总物质的量保持不变 |
7.下列说法正确的是( )
| A. | 强电解质溶液一定比弱电解质溶液导电能力强 | |
| B. | BaSO4是弱电解质 | |
| C. | 蔗糖、CO2是非电解质 | |
| D. | 盐酸能导电,所以盐酸是电解质 |
 .
.
 .
.