题目内容
12.W、X、Y、Z是原子序数依次增大的同一短周期元素,W、X是金属元素,Y、Z是非金属元素.(1)W、X各自的最高价氧化物对应的水化物可以反应生盐和水,该反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(2)W与Y 可形成化合物W2Y,该化合物的电子式为
 .
.(3)Y的单质与Fe3O4高温下发生反应的化学方程式为8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe.
(4)比较Y、Z气态氢化物的稳定性HCl>H2S(用分子式表示)
(5)W、X、Y、Z四种元素简单离子的离子半径由大到小的顺序是:S 2->Cl->Na+>Al 3+.
分析 W、X、Y、Z是原子序数依次增大的同一周期元素,W、X是金属元素,Y、Z是非金属元素.
(1)W、X各自的氧化物对应的水化物可以反应生成盐和水,可推知W为Na、X为Al;
(2)W(Na)与Y可形成化合物W2Y,Y表现-2价,则Y为S;
(3)Al单质与Fe3O4高温下发生置换反应生成Fe与氧化铝;
(4)同周期自左而右元素非金属性增强,非金属性越强,氢化物越稳定;
(5)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大.
解答 解:W、X、Y、Z是原子序数依次增大的同一周期元素,原子序数均小于18,W、X是金属元素,Y、Z是非金属元素
(1)W、X为金属,其最高价氧化物对应的水化物为碱,且两种碱可以反应生成盐和水,则为NaOH和Al(OH)3,二者反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O;
(2)W(Na)与Y可形成化合物W2Y,Y表现-2价,则Y为S,Na2S的电子式为: ,故答案为:
,故答案为: ;
;
(3)Al单质与Fe3O4高温下发生置换反应生成Fe与氧化铝,反应方程式为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe,故答案为:8Al+3Fe3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Fe;
(4)同一周期元素中,元素的非金属性随着原子序数的增大而增强,元素的非金属性越强,其氢化物越稳定,所以稳定性为HCl>H2S,故答案为:HCl;H2S;
(5)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径大小顺序是:S 2->Cl->Na+>Al3+,
故答案为:S 2-;Cl-;Na+;Al3+.
点评 本题考查结构性质位置关系应用,涉及电子式、半径比较、元素周期律、离子方程式书写等,正确推断元素是解本题关键,注意掌握微粒半径大小的比较方法,熟练掌握元素化合物性质.

| A. | 定量检验C2H5Cl时,将C2H5Cl和NaOH溶液混合共热后,加盐酸酸化 | |
| B. | 为提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液酸化 | |
| C. | 鉴定检测液中是否有Fe2+时,用硝酸酸化,再加KSCN溶液 | |
| D. | 鉴别溶液中是否含有SO42-可用盐酸酸化 |
| A. | 醋酸 | B. | 聚乙烯 | C. | 乙醇 | D. | 苯 |
| A. | 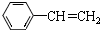 | B. |  | C. | 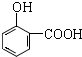 | D. | HC≡CCH=CHC≡CH |
| A. | 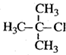 2-甲基-2-氯丙烷 | B. | 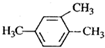 1,3,4-三甲苯 | C. | 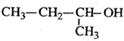 2-甲基-1-丙醇 | D. | 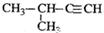 2-甲基-3-丁炔 |
(1)写出NaCN的电子式Na+
 ,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.
,偏碱性条件下,氰化钠溶液的CN-被双氧水氧化为HCO3-,同时放出NH3,该反应的离子方程式:CN-+H2O2+H2O═NH3↑+HCO3-.(2)Cu2+可作为双氧水氧化CN-中的催化剂.某兴趣小组要探究Cu2+对双氧水氧化CN-是否起催化作用,请你完成下实验方案.填写实验步骤、实验现象和结论(己知:CN-浓度可用离子色谱仪测定)
| 步骤:分别取等体积、等浓度的含氰废水于甲、乙两支试管中,再分别加入等体积、等浓度的双氧水溶液,只向甲试管中加入少量的无水硫酸铜粉末,用离子色谱仪测定相同反应时间内两支试管中的CN-浓度 | 现象与结论: 若若甲试管中的CN-浓度小于乙试管中的CN-浓度,则Cu2+对双氧水破氰反应起催化作用 若若两试管中的CN-浓度相同,则Cu2+对双氧水破氰反应不起催化作用 |
| A. | 电池充电时其正极应与外电源的负极相连而成为阴极 | |
| B. | 氢氧燃料电池(碱性介质)的正极反应式:O2+4e-→2O2- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜 | |
| D. | 铁件上镀铜时,将铁件与电源的负极相连 |