题目内容
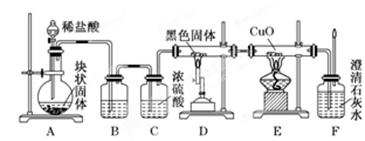
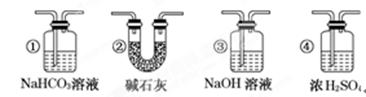
(10分)某化学活动小组设计如图所示装置(部分夹持装置已略去)实验,以探究潮湿的Cl2与Na2CO3反应的产物。

(1)写出装置A中发生反应的化学方程式:________ _____________。
(2)写出试剂Y的名称:__________________ _________________。
(3)将C中反应后的固体物质分成两等份分装于两支试管中,
①向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,写出产生此现象的离子方程式:________ ____________;由此现象推断固体产物中含有______ ____(填化学式,下同);
②向另一支试管中滴加过量的稀硝酸,有无色无味的气体产生,溶液澄清,再向溶液滴加过量的AgNO3溶液,溶液变浑浊,经过滤、洗涤、干燥,得到14.35g固体,由此现象推断固体产物中含有____ ____
(4)已知C中有0.1molCl2参加反应,D中收集到的气体是氯的一种氧化物,由(4)中现象及数据可推知,C中反应的化学方程式为________ ___________。

(1)写出装置A中发生反应的化学方程式:________ _____________。
(2)写出试剂Y的名称:__________________ _________________。
(3)将C中反应后的固体物质分成两等份分装于两支试管中,
①向其中一支试管中加蒸馏水至固体完全溶解后,滴加BaCl2溶液,无明显现象,再滴加NaOH溶液变浑浊,写出产生此现象的离子方程式:________ ____________;由此现象推断固体产物中含有______ ____(填化学式,下同);
②向另一支试管中滴加过量的稀硝酸,有无色无味的气体产生,溶液澄清,再向溶液滴加过量的AgNO3溶液,溶液变浑浊,经过滤、洗涤、干燥,得到14.35g固体,由此现象推断固体产物中含有____ ____
(4)已知C中有0.1molCl2参加反应,D中收集到的气体是氯的一种氧化物,由(4)中现象及数据可推知,C中反应的化学方程式为________ ___________。
(1) MnO2+4H++2Cl-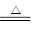 Mn2++Cl2↑+2H2O(2分)
Mn2++Cl2↑+2H2O(2分)
(2)饱和食盐水(或饱和氯化钠溶液)(2分)
(3)①HCO3-+Ba2++OH-=BaCO3↓+H2O(各2分); NaHCO3 ②NaCl (各1分)
(4)2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl +Cl2O↑(2分)
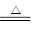 Mn2++Cl2↑+2H2O(2分)
Mn2++Cl2↑+2H2O(2分) (2)饱和食盐水(或饱和氯化钠溶液)(2分)
(3)①HCO3-+Ba2++OH-=BaCO3↓+H2O(各2分); NaHCO3 ②NaCl (各1分)
(4)2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl +Cl2O↑(2分)
(1)A装置是制取氯气的,所以方程式是 MnO2+4H++2Cl-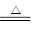 Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(2)由于生成的氯气中含有氯化氢,而氯化氢能与碳酸钠反应,所以B中试剂是除去氯气中的氯化氢的,选择的试剂是饱和食盐水。
(3)①加入氯化钡没有白色沉淀生成,所以不含有CO32-。但滴加NaOH溶液变浑浊,所以含有HCO3-,因此是是碳酸氢钠,反应的方程式是HCO3-+Ba2++OH-=BaCO3↓+H2O。
②加入硝酸酸化的硝酸银能产生白色沉淀,因此沉淀是氯化银,所以一定含有氯化钠。
(4)白色沉淀氯化银是0.1mol,所以生成的氯化钠也是0.1mol。参加反应的氯气是0.1mol,所以根据电子得失守恒可知,该氧化物中氯元素的化合价是+1价,所以该氧化物的化学式是Cl2O,因此反应的方程式是2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl +Cl2O↑。
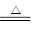 Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。(2)由于生成的氯气中含有氯化氢,而氯化氢能与碳酸钠反应,所以B中试剂是除去氯气中的氯化氢的,选择的试剂是饱和食盐水。
(3)①加入氯化钡没有白色沉淀生成,所以不含有CO32-。但滴加NaOH溶液变浑浊,所以含有HCO3-,因此是是碳酸氢钠,反应的方程式是HCO3-+Ba2++OH-=BaCO3↓+H2O。
②加入硝酸酸化的硝酸银能产生白色沉淀,因此沉淀是氯化银,所以一定含有氯化钠。
(4)白色沉淀氯化银是0.1mol,所以生成的氯化钠也是0.1mol。参加反应的氯气是0.1mol,所以根据电子得失守恒可知,该氧化物中氯元素的化合价是+1价,所以该氧化物的化学式是Cl2O,因此反应的方程式是2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl +Cl2O↑。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是 ;
MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是 ; 2BN + 3H2O。(已知:BN高温下能被空气氧化,不溶于水;B2O3难溶于冷水但可溶于热水。)
2BN + 3H2O。(已知:BN高温下能被空气氧化,不溶于水;B2O3难溶于冷水但可溶于热水。)