题目内容
【题目】黄铜矿不仅可用于火法炼铜,也可用于湿法炼铜,湿法可同时生产铜、磁性氧化铁和用于橡胶工业的一种固体物质A,流程如下:
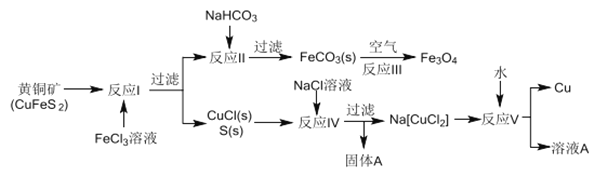
(1)黄铜矿中Cu 的化合价是______,反应I中65gFeC13 可氧化________mol CuFeS2。
(2)工业生产中的过滤操作多采用倾析法分离出固体物质,下列适合用倾析法的有______。
A.沉淀的颗粒较大 B.沉淀容易沉降 C.沉淀呈胶状 D.沉淀呈絮状
(3)在反应Ⅱ中,计算NaHCO3饱和溶液(其中CO32-平衡浓度为1.2×10-3mol/L)可产生FeCO3沉淀时的最小Fe2+浓度是_________(己知FeCO3的Ksp=3.0×10-11)
(4)反应Ⅲ是在设备底部鼓入空气,高温氧化锻烧法来制备磁性氧化铁,写出对应的化学方程式_________________。
(5)固体物质A的成分________(写名称)。
(6)潮湿的FeCO3固体若不及时灼烧处理会在空气中逐渐变红,写出相关的化学方程式:_______________。
(7)本流程中可实现循环使用的物质除了水外,还有_____________
【答案】 +2 0.1 AB 2.5×10-8mol/L 6FeCO3+O2![]() 2Fe3O4+6CO2 硫 6FeCO3+O2+6H2O==4Fe(OH)3+4CO2 氯化钠
2Fe3O4+6CO2 硫 6FeCO3+O2+6H2O==4Fe(OH)3+4CO2 氯化钠
【解析】 (1)根据化合价的代数和为0,黄铜矿CuFeS2中Cu 的化合价为+2价,Fe为+2价,S为-2价;65gFeC13 的物质的量为![]() =0.4mol,反应后得到0.4mol电子,根据流程图,反应后生成CuCl和S,只有S元素被氧化,根据得失电子守恒,能够氧化0.1mol CuFeS2,故答案为:+2;0.1;
=0.4mol,反应后得到0.4mol电子,根据流程图,反应后生成CuCl和S,只有S元素被氧化,根据得失电子守恒,能够氧化0.1mol CuFeS2,故答案为:+2;0.1;
(2) 沉淀的颗粒较大,静止后容易沉降至容器底部,常用倾析法分离,沉淀呈胶状或絮状,静止后不容易沉降,不能采取倾析法分离,故选AB;
(3)在反应Ⅱ中, NaHCO3饱和溶液中CO32-平衡浓度为1.2×10-3mol/L,可产生FeCO3沉淀时的最小Fe2+浓度为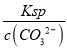 =
=![]() =2.5×10-8mol/L,故答案为:2.5×10-8mol/L;
=2.5×10-8mol/L,故答案为:2.5×10-8mol/L;
(4)反应Ⅲ中,在设备底部鼓入空气,碳酸亚铁被氧化生成磁性氧化铁(Fe3O4),反应的化学方程式为6FeCO3+O2![]() 2Fe3O4+6CO2,故答案为:6FeCO3+O2
2Fe3O4+6CO2,故答案为:6FeCO3+O2![]() 2Fe3O4+6CO2;
2Fe3O4+6CO2;
(5)根据流程图,加入氯化钠溶液将CuCl转化为络合物,固体物质A为硫,故答案为:硫;
(6)亚铁离子具有还原性,在潮湿的空气中FeCO3固体被氧化变红,反应的化学方程式6FeCO3+O2+6H2O==4Fe(OH)3+4CO2,故答案为:6FeCO3+O2+6H2O==4Fe(OH)3+4CO2;
(7)根据流程图,溶液A中含有氯化钠,可以参与循环使用,故答案为:氯化钠。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案【题目】1915年诺贝尔物理学奖授予Henry Bragg 和 Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献。
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
晶体 | NaCl | KCl | CaO |
晶格能/(kJ·mol1) | 786 | 715 | 3401 |
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是______,Na核外有__________种不同的能级。
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可用右图简单表示,其中配位键和氢键均采用虚线表示。
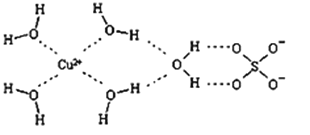
①SO42 中S的杂化类型是____________,与其互为等电子体的离子有___________(任写两种)
②已知 [Cu(NH3)4]2+ 具有对称的空间构型,[Cu(NH3)4]2+ 中的两个NH3被 Cl 取代,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为_______________。
③写出基态Cu2+ 的价层电子排布式:_________;金属铜采取_________堆积方式,已知Cu原子的半径为 r pm,NA 表示阿伏加德罗常数的值,金属铜的密度是_______________g/cm3(列出计算式)