题目内容
【题目】化合物Ⅳ为一种重要化工中间体,其合成方法如下: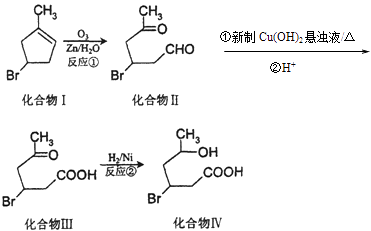
(1)化合物Ⅰ在核磁共振氢谱图吸收峰个数为;反应②的反应类型为 .
(2)化合物Ⅱ与新制Cu(OH)2悬浊液反应,写出该反应的化学方程式 .
(3)化合物I在NaOH醇溶液中加热反应得到化合物X,X的结构简式可能是 . (写出任意一种的结构简式).
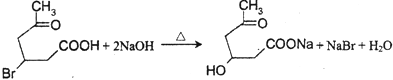
(4)化合物III与足量NaOH水溶液加热反应的化学方程式为 .
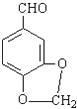
(5)异黄樟油素 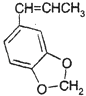 发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为 .
发生类似反应①的反应,得到乙醛和化合物Y,Y的结构简式为 .
(6)有关上述化合物,说法不正确的是
A.1mol化合物Ⅲ,最多可与2molH2反应
B.化合物Ⅳ在一定条件下能与HBr反应
C.化合物Ⅰ能使酸性高锰酸钾溶液褪色
D.化合物Ⅳ在一定条件下能发生缩聚反应
E.化合物Ⅱ分子式为C6H11O2Br.
【答案】
(1)5;加成反应(或还原反应)
(2)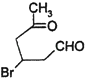 +2Cu(OH)2
+2Cu(OH)2![]()
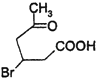 +Cu2O↓+2H2O
+Cu2O↓+2H2O
(3)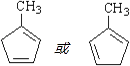
(4)
(5)
(6)AE
【解析】解:(1)根据化合物Ⅰ的结构简式可知,其分子中含有5种等效H,则核磁共振氢谱图吸收峰个数为5;反应②中C=O变成C﹣O键,该反应属于加成反应,也属于还原反应,所以答案是:5;加成反应(或还原反应);(2)化合物Ⅱ为 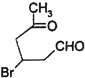 ,其分子中含有醛基,能够与新制氢氧化铜浊液发生反应生成
,其分子中含有醛基,能够与新制氢氧化铜浊液发生反应生成 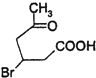 ,反应的化学方程式为:
,反应的化学方程式为:  +2Cu(OH)2
+2Cu(OH)2![]()
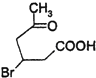 +Cu2O↓+2H2O,
+Cu2O↓+2H2O,
所以答案是: 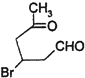 +2Cu(OH)2
+2Cu(OH)2![]()
 +Cu2O↓+2H2O;(3)化合物I在NaOH的醇溶液中反应发生消去反应,可得到两种有机物,结构简式分别为:
+Cu2O↓+2H2O;(3)化合物I在NaOH的醇溶液中反应发生消去反应,可得到两种有机物,结构简式分别为: 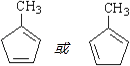 ,
,
所以答案是: 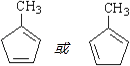 ;(4)化合物III中含有﹣COOH和﹣Br,在碱性条件下反应生成﹣COONa和﹣OH,则反应的方程式为:
;(4)化合物III中含有﹣COOH和﹣Br,在碱性条件下反应生成﹣COONa和﹣OH,则反应的方程式为: 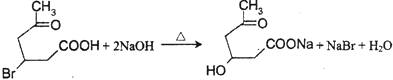 ,
,
所以答案是: 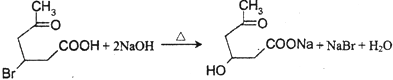 ;(5)异黄樟油素(
;(5)异黄樟油素( 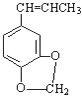 )发生类似反应①的反应,应为C=C被氧化分别生成醛或酮,则生成的化合物Ⅵ的结构简式为:
)发生类似反应①的反应,应为C=C被氧化分别生成醛或酮,则生成的化合物Ⅵ的结构简式为: 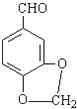 ,
,
所以答案是:  ;(6)A.1mol化合物Ⅲ(
;(6)A.1mol化合物Ⅲ( 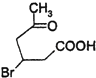 )中含有1mol碳碳双键,最多可与1molH2反应,故A错误;
)中含有1mol碳碳双键,最多可与1molH2反应,故A错误;
B.化合物Ⅳ中含有羟基,在一定条件下能与HBr发生取代反应,故B正确;
C.化合物Ⅰ中含有碳碳双键,能被酸性高锰酸钾溶液氧化,从而使酸性高锰酸钾溶液褪色,故C正确;
D.化合物Ⅳ中含有羟基和羧基,在一定条件下能发生缩聚反应生成高分子化合物,故D正确;
E.根据化合物Ⅱ的结构简式可知,其分子式为C6H9O2Br,故E错误;
所以答案是:AE.

【题目】已知β锂辉矿(主要成分为LiAlSi2O6 , 还含有FeO、MgO、CaO等杂质),下面是以锂辉矿为原料来制取金属锂的一种工艺流程.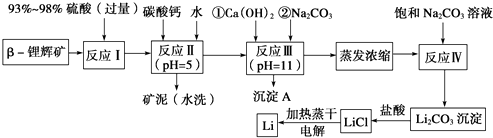
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
请回答下列问题:
(1)为了提高β锂辉矿浸出率可采取措施有 .
(2)反应Ⅰ发生主反应:LiAlSi2O6+H2SO4(浓Li2SO4+++H2O,根据题意配平上述方程式.
(3)反应Ⅱ加入碳酸钙的作用是 .
(4)反应Ⅲ中生成沉淀A成分: . (填化学式)
(5)蒸发浓缩过程中主要发生离子反应方程式: .
(6)洗涤所得Li2CO3沉淀要使用(选填“热水”或“冷水”),你选择的理由是 .
(7)电解熔融氯化锂生产锂时,阳极产生的Cl2中会混有少量O2 , 用电极反应式说明原因 .