题目内容
【题目】常温下,Ksp(BaSO4)=1.0×10-10,Ksp(SrSO4)=3.0×10-7向20mL0.1mo1·L-1BaCl2溶液中滴加0.1mol·L-1的Na2SO4溶液,金属离子浓度与硫酸钠溶液体积的关系如图所示,已知:pM=-lgc(M2+)。下列说法正确的是( )
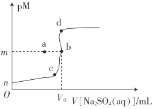
A.图像中,V0=20,m=5
B.在b点加少量BaCl2固体,Ksp(BaSO4)增大
C.若BaCl2溶液体积仍为20mL,浓度变为0.2mo1·L-1,则b点向a点迁移
D.若用SrCl2溶液替代BaCl2溶液,则b点向d点迁移
【答案】A
【解析】
A.图象中,V0=20时,氯化钡和硫酸钠恰好完全反应,则c(Mg2+)=c(SO42-)=![]() mol/L,m=5,故A正确;
mol/L,m=5,故A正确;
B.溶度积只受温度的影响,加入氯化钡固体,溶度积不变,故B错误;
C.若BaCl2溶液体积仍为20mL,浓度变为0.2mo1L-1,完全反应时,应加入40mL硫酸钠,则V0变大,故C错误;
D.若用SrCl2溶液替代BaCl2溶液,完全反应,因Ksp(SrSO4)较大,则c(Sr2+)较大,pM应减小,故D错误;
故答案为A。

练习册系列答案
相关题目