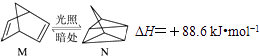
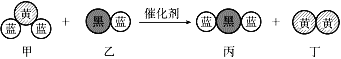
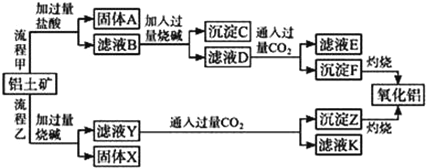
题目内容
【题目】研究PM 2.5、SO2、NOx等,对监测空气质量具有重要意义.取某样本用蒸馏水处理制成待测液,其中所含离子的化学组分及其浓度如下表:
离子 | K+ | Na+ | NH4+ | H+ | SO42﹣ | NO3﹣ | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣6 | 2×10﹣5 | a | 2×10﹣5 | 3×10﹣5 | 2×10﹣5 |
请回答下列问题:
(1)根据表中数据计算此待测液中c(H+)浓度a为________mol/L.
(2)NOx是汽车尾气中的主要污染物之一.
①汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是__________.
②NOx能形成酸雨,由NO2形成酸雨的主要反应是______________(写化学方程式).
(3)为减少SO2的排放,常采取的措施有:
①在燃煤中加入生石灰可以起到固硫的作用,SO2被吸收后转化成一种硫元素的最高价态的化合物,该化合物常作为豆腐生产的原料,它在豆腐生产中的作用是___________.
②吸收烟气中的SO2,以下物质可作吸收剂的是_______(填序号);
a.NaOH b.H2SO4 c.NaHSO3 d. Na2SO3
硫酸工业中的尾气SO2可以循环利用,写出SO2转化为SO3反应的化学方程式_______.
【答案】 6×10﹣5 N2+O2![]() 2NO 3NO2+H2O═2HNO3+NO 使胶体聚沉 ad 2SO2+O2
2NO 3NO2+H2O═2HNO3+NO 使胶体聚沉 ad 2SO2+O2![]() 2SO3
2SO3
【解析】(1)根据溶液中存在电荷守恒:c(K+)+c(Na+)+c(NH4+)+c(H+)=2c(SO42-)+c(NO3-)+C(Cl-),结合图表数据计算得到氢离子浓度c(H+)=2×2×10﹣5+3×10﹣5+2×10﹣5-4×10﹣6-6×10﹣6-2×10﹣5=6×10﹣5 molL﹣1,正确答案:6×10﹣5。
(2)①汽车发动机工作时的高温会引发N2和O2反应,反应的化学方程式是N2+O2![]() 2NO ;正确答案:N2+O2
2NO ;正确答案:N2+O2![]() 2NO。
2NO。
②NO2与水反应生成硝酸和一氧化氮,硝酸为酸雨的主要成分,由NO2形成酸雨的主要反应是3NO2+H2O═2HNO3+NO;正确答案:3NO2+H2O═2HNO3+NO。
(3)①在燃煤中加入生石灰可以起到固硫的作用,是氧化钙和二氧化硫反应生成亚硫酸钙,亚硫酸钙被氧气氧化为硫酸钙,豆浆为胶体,加入硫酸钙电解质后,使胶体聚沉;正确答案:使胶体聚沉。
②二氧化硫是酸性氧化物,氢氧化钠溶液可以吸收二氧化硫,生成亚硫酸氢钠或亚硫酸钠,a正确;H2SO4 与二氧化硫不反应,b错误;亚硫酸氢钠溶液与二氧化硫不反应,c错误;Na2SO3能够与二氧化硫反应生成亚硫酸氢钠,可以作吸收剂,d正确;正确选项ad。 硫酸工业中的尾气SO2可以循环利用,写出SO2转化为SO3反应的化学方程式2SO2+O2![]() 2SO3;正确答案:2SO2+O2
2SO3;正确答案:2SO2+O2![]() 2SO3。
2SO3。

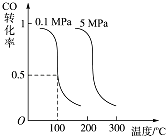
【题目】一定条件下存在反应C(s)+H2O(g)![]() CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法错误的是( )
CO(g)+H2(g) △H>0,向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。下列说法错误的是( )
容器 | 甲 | 乙 | 丙 |
容积 | 0.5 L | 0.5 L | V |
温度 | T1℃ | T2℃ | T1℃ |
起始量 | 2 molC 1 molH2O | 1 molCO 1 molH2 | 4 molC 2molH2O |

A. 甲容器中,反应在前15 min的平均速率v(H2)=0.1mol·L-1·min-1
B. 丙容器的体积V>0.5 L
C. 当温度为T1℃时,反应的平衡常数K=4.5
D. 乙容器中,若平衡时n(H2O)=0.4 mol,则T2< T1
【题目】某兴趣小组设计了如图所示装置(部分夹持装置已略去)进行实验探究. 【实验一】探究影响化学反应速率的因素.
圆底烧瓶中装锌片(两次实验中所用锌片大小和外形相同)、恒压分液漏斗中装稀硫酸,以生成20.0mL气体为计时终点,结果为t1>t2 .
序号 | V(H2SO4)/mL | c(H2SO4)/molL﹣1 | t/s |
I | 40 | 1 | t1 |
II | 40 | 3 | t2 |
检查该装置气密性的方法是 .
比较实验I和Ⅱ可以得出的结论是 .
【实验二】探究铁的电化学腐蚀.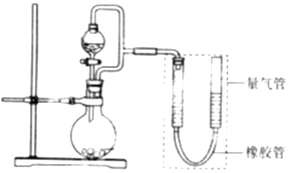
①圆底烧瓶中装铁粉和碳粉混合物,恒压分液漏斗中装稀硫酸,打开活塞加入稀硫酸后量气管中出现的现象是:左侧液面右侧液面(选填“上升”、“下降”).
②圆底烧瓶中装与①相同量的铁粉和碳粉混合物,恒压分液漏斗中装食盐水,打开活塞加入食盐水后,你预测量气管中出现的现象是: . 实际观察到的现象可能与预测并不一致,装置气密性良好,原因是 .