题目内容
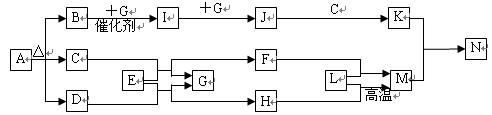
(15分)下图中所有物质均为中学化学常见物质,F、H是气体单质,Z是金属单质,Y中阳离子与阴离子个数比为2 :1,化合物X、Y、A、D、E、G的焰色反应均为黄色,I是白色胶状沉淀。
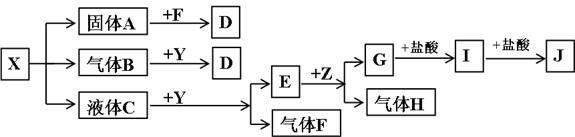
请回答下列问题:
(1)Y的电子式 。关于Y的说法正确的是 。
A.Y是酸性氧化物 B. Y是过氧化物 C. Y是碱性氧化物 D. Y可以作漂白剂
(2)J溶液中离子浓度由大到小的顺序为_____________________________________________。
(3)写出G与盐酸反应生成I的离子方程式 。
(4)写出B与Y反应的化学方程式 。
(5)将一定量的黄绿色气体W2通入到E的溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含W元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化如图所示。该反应中转移电子的物质的量是 mol,该反应总反应的化学方程式为
。

请回答下列问题:
(1)Y的电子式 。关于Y的说法正确的是 。
A.Y是酸性氧化物 B. Y是过氧化物 C. Y是碱性氧化物 D. Y可以作漂白剂
(2)J溶液中离子浓度由大到小的顺序为_____________________________________________。
(3)写出G与盐酸反应生成I的离子方程式 。
(4)写出B与Y反应的化学方程式 。
(5)将一定量的黄绿色气体W2通入到E的溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含W元素的离子,其中两种离子的物质的量(n)与反应时间(t)的变化如图所示。该反应中转移电子的物质的量是 mol,该反应总反应的化学方程式为
。

(1)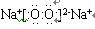 (2分) B D (2分,错选项倒扣分,每个1分)
(2分) B D (2分,错选项倒扣分,每个1分)
(2)C(Cl-)>C(Al3+)>C(H+)>C(OH-)(2分)
(3)AlO2- + H+ + H2O = Al(OH)3↓ (2分)
(4)Na2O2 + +SO2 = Na2SO4 (2分)
(5)0.14(2分) 5Cl2 + 10NaOH =" 7NaCl" +2NaClO + 5H2O + NaClO3(3分,条件加热1分)
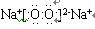 (2分) B D (2分,错选项倒扣分,每个1分)
(2分) B D (2分,错选项倒扣分,每个1分)(2)C(Cl-)>C(Al3+)>C(H+)>C(OH-)(2分)
(3)AlO2- + H+ + H2O = Al(OH)3↓ (2分)
(4)Na2O2 + +SO2 = Na2SO4 (2分)
(5)0.14(2分) 5Cl2 + 10NaOH =" 7NaCl" +2NaClO + 5H2O + NaClO3(3分,条件加热1分)
略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
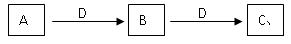
 : 。
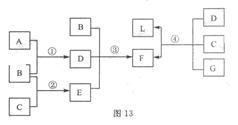
: 。 L;固体单C可以在B中燃烧;A、B、G通常为气态单质。请回答有关问题:
L;固体单C可以在B中燃烧;A、B、G通常为气态单质。请回答有关问题: