题目内容
6.从海带中提取碘,有甲、乙两种实验方案如图1:已知:3I2+6NaOH=5NaI+NaIO3+3H2O.请回答:(1)步骤X使用分液漏斗前须检漏,检漏方法为向分液漏斗中加入少量水,检查下口旋塞处是否漏水,将漏斗倒转过来,检查上口玻璃塞是否漏水.
(2)用图所示装置进行蒸馏.指出如图所示实验装置 中的任意两处错误:①温度计水银球位置太低,应位于蒸馏烧瓶支管口处;②烧杯加热未使用石棉网或冷凝管冷却水流方向反了.
(3)进行上述操作时,使用水浴加热更好的原因是均匀受热,易于控制温度;最后碘晶体在蒸馏烧瓶里聚集.
(4)下列有关步骤Y的说法,正确的是AB.
A.应控制 NaOH 溶液的浓度和体积 B.将碘转化成离子进入水层 C.主要是除去海带浸取原液中的有机杂质
D.NaOH 溶液可以由乙醇代替
(5)方案乙在上层溶液中加入H2SO4溶液得到I2的水溶液发生的反应方程式是:5NaI+NaIO3+3H2SO4=3I2+3Na2SO4+3H2O;
(6)操作Z的名称是过滤.
(7)工业中采用方案乙从海带中提取碘,方案甲中采用蒸馏不合理,理由是碘单质易升华,会导致碘损失.
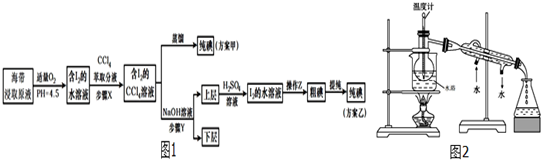
分析 海带浸取液中通入氧气调节溶液PH,得到韩I2的水溶液,加入有机溶剂四氯化碳萃取分液得到韩I2的CCl4溶液,方案乙是:步骤Y利用氢氧化钠溶液吸收分液得到上层溶液中是NaI和NaIO3,加入H2SO4溶液发生归中反应得到I2的水溶液,过滤得到粗碘蒸馏提纯得到纯净碘单质,方案甲是直接蒸馏得到碘单质,
(1)检查分液漏斗是否漏水,需要分别检查瓶塞、旋塞是否漏水;
(2)蒸馏装置温度计水银球应在蒸馏烧瓶支管口处测定馏出成分的沸点,烧杯加热需要垫石棉网均匀加热,冷凝管水流方向应逆流;
(3)碘易升华,需要水浴加热控制温度,水浴加热均匀,碘单质生成蒸气,遇冷冷凝在蒸馏烧瓶中;
(4)A.反应3I2+6NaOH═5NaI+NaIO3+3H2O中,需要浓氢氧化钠溶液;
B.碘单质与氢氧化钠反应生成了碘化钠、碘酸钠;
C.该操作的主要目的是将碘单质转化成碘酸钠、碘化钠,便于后续分离出碘单质;
D.乙醇易溶于水和四氯化碳,仍然无法分离出碘单质.
(5)方案乙在上层溶液中是NaI和NaIO3,加入H2SO4溶液发生归中反应得到I2的水溶液;
(6)碘单质不溶于水,可以通过过滤操作分离出碘单质;
(7)从碘单质易升华角度分析.
解答 解:(1)检查分液漏斗是否漏水的操作方法为:向分液漏斗中加入少量蒸馏水,检查旋塞处是否漏水;将漏斗倒转过来,检查玻璃塞是否漏水,
故答案为:向分液漏斗中加入少量蒸馏水,检查旋塞处是否漏水,将漏斗倒转过来,检查玻璃塞是否漏水;
(2)蒸馏装置温度计水银球应在蒸馏烧瓶支管口处测定馏出成分的沸点,烧杯加热需要垫石棉网均匀加热,冷凝管水流方向应逆流,分析装置图可知,操作错误为:温度计插入液面以下,烧杯未垫石棉网,冷凝管水流方向顺流,
故答案为:温度计水银球位置太低,应位于蒸馏烧瓶支管口处;烧杯加热未使用石棉网或冷凝管冷却水流方向反了;
(3)碘易升华,需要水浴加热控制温度,水浴加热受热均匀,便于控制温度,碘单质生成蒸气,遇冷冷凝在蒸馏烧瓶中,
故答案为:均匀受热,易于控制温度;蒸馏烧瓶;
(4)A.发生反应3I2+6NaOH═5NaI+NaIO3+3H2O中,需要浓氢氧化钠溶液,所以应控制NaOH溶液的浓度和体积,故A正确;
B.根据反应3I2+6NaOH═5NaI+NaIO3+3H2O可知,步骤Y将碘转化成离子进入水层,故B正确;
C.该操作的主要目的是将碘单质转化成碘酸钠、碘化钠,将碘转化成离子进入水层,不是除去有机杂质,故C错误;
D.乙醇易溶于水和四氯化碳,将氢氧化钠换成乙醇,仍然无法分离出碘单质,故D错误;
故答案为:AB;
(5)方案乙在上层溶液中是NaI和NaIO3,加入H2SO4溶液发生归中反应得到I2的水溶液,反应的化学方程式为:5NaI+NaIO3+3H2SO4=3I2+3Na2SO4+3H2O,
故答案为:5NaI+NaIO3+3H2SO4=3I2+3Na2SO4+3H2O;
(6)步骤Z将碘单质和水分离,由于碘单质不溶于水,可通过过滤操作完成,故答案为:过滤;
(7)方案甲中采用蒸馏操作,由于碘单质容易升华,会导致碘单质损失,所以甲方案不合理,故答案为:碘单质易升华,会导致碘损失.
点评 本题考查物质的分离与提纯方法的综合应用,题目难度中等,试题涉及的知识点较多、综合性较强,充分考查学生的分析、理解能力及化学实验能力,明确实验原理为解答关键,注意熟练掌握化学实验基本操作方法.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 原子半径:A<B | B. | 原子序数:A>B | ||
| C. | 原子最外层电子数:B>A | D. | 元素所在的周期数:A>B |
| A. | 青蒿素的摩尔质量为282 | |
| B. | 6.02×1023个青蒿素分子的质量约为282g | |
| C. | 1 mol青蒿素的质量为282g•mol-1 | |
| D. | 282g青蒿素中含有15个碳原子 |
| A. | ①⑤③⑥⑦④② | B. | ①⑤③④⑥⑦② | C. | ①③④⑥⑦⑤② | D. | ①③⑤⑥⑦④② |
| A. | 0.01 | B. | 0.02 | C. | 0.03 | D. | 0.06 |
| A. | 溶解、结晶、过滤、升华 | B. | 加热(升华)、溶解、过滤、蒸发(结晶) | ||
| C. | 加热(升华)、溶解、蒸馏、结晶 | D. | 溶解、过滤、加热(升华)、蒸发(结晶) |
| A. | 胆矾、绿矾 | B. | 苏打、小苏打 | C. | 生石灰、碱石灰 | D. | 烧碱、苛性钠 |