题目内容
【题目】下列混合物的物质的量一定时,组内各物质按任意比混合,完全燃烧时耗O2的量不变的是
A. 甲烷、甲醇、甲醛 B. 丙烯酸(CH2=CH-COOH)、乙烯、乙醇
C. 丙烯、2-丁烯、环已烷 D. 乙炔、苯、1,3-丁二烯
【答案】B
【解析】A、CH4的(x+![]() -
-![]() )=1+1=2,甲醇的(x+
)=1+1=2,甲醇的(x+![]() -
-![]() )=1+1-0.5=1.5,甲醛的(x+
)=1+1-0.5=1.5,甲醛的(x+![]() -
-![]() )=1+0.5=0.5,三者(x+
)=1+0.5=0.5,三者(x+![]() -
-![]() )值不相等,故A错误;B、丙烯酸的(x+
)值不相等,故A错误;B、丙烯酸的(x+![]() -
-![]() )=3+1-1=3,乙烯的(x+
)=3+1-1=3,乙烯的(x+![]() -
-![]() )=1+2=3,乙醇的(x+
)=1+2=3,乙醇的(x+![]() -
-![]() )=2+1.5-0.5=3,三者(x+
)=2+1.5-0.5=3,三者(x+![]() -
-![]() )值相等,故B正确;C、丙烯的(x+
)值相等,故B正确;C、丙烯的(x+![]() -
-![]() )=3+1.5=4.5,2-丁烯的(x+
)=3+1.5=4.5,2-丁烯的(x+![]() -
-![]() )=4+2=6,环己烷的(x+
)=4+2=6,环己烷的(x+![]() -
-![]() )=6+3=9,三者(x+
)=6+3=9,三者(x+![]() -
-![]() )值不相等,故C错误;D、乙炔的(x+
)值不相等,故C错误;D、乙炔的(x+![]() -
-![]() )=2+0.5=2.5,苯的(x+
)=2+0.5=2.5,苯的(x+![]() -
-![]() )=6+1.5=7.5,1-3-丁二烯的(x+
)=6+1.5=7.5,1-3-丁二烯的(x+![]() -
-![]() )=4+1.5=5.5,三者(x+
)=4+1.5=5.5,三者(x+![]() -
-![]() )值不相等,故D错误;故选B。
)值不相等,故D错误;故选B。

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】五种短周期元素A、B、C、D、E的性质及结构信息如下:
① 原子半径A>B>C>D>E;
② 五种元素之间形成的常见的四种分子如下:
甲 | 乙 | 丙 | 丁 | |
比例模型 |
|
|
|
|
组成元素 | D、E | B、E | A、D、E | C、E |
电子总数 | 10 | 18 | 26 | 10 |
请根据上述信息回答下列问题:
(1)A元素的单质与物质甲发生反应的离子方程式为__________,其化学反应平衡常数的表达式为_______。
(2)戊与乙互为同系物,有五种同分异构体,戊的分子式为_____,己与乙具有相同的电子数,与甲含有的元素种类相同,己分子的结构式为_______。
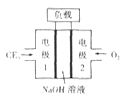
(3)C与E元素组成的CE3与液氮可组成燃料电池,产物均为无污染的物质,可用于驱动潜艇,燃料电池装置如下图所示。该电池的负极反应式为_____。电池工作时OH-向_____移动(填“正极”或“负极”)。
(4)B与D组成的一种物质在自然界中可循环,循环时其与CaCO3反应。已知Ksp(CaCO3)=2.8×10-9,现将CaCl2溶液与Na2CO3溶液等体积混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀的最小浓度为__________(忽略混合前后溶液的体积变化)。


