题目内容
【题目】下列反应中,非金属元素被还原的是( )
A. MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2OB. H2+CuO
MnCl2+Cl2↑+2H2OB. H2+CuO![]() Cu+H2O
Cu+H2O
C. 2FeCl2+Cl2===2FeCl3D. 2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
【答案】C
【解析】
非金属元素被还原,即非金属元素发生化合价降低的还原反应,由此分析解答。
A. MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O反应中,Cl元素化合价从-1价升高到0价,被氧化,不符合题意,A项错误;
MnCl2+Cl2↑+2H2O反应中,Cl元素化合价从-1价升高到0价,被氧化,不符合题意,A项错误;
B. H2+CuO![]() Cu+H2O反应中,H元素化合价从0价升高到+1价,被氧化,不符合题意,B项错误;
Cu+H2O反应中,H元素化合价从0价升高到+1价,被氧化,不符合题意,B项错误;
C. 2FeCl2+Cl2===2FeCl3反应中,Cl元素化合价从0价降低到-1价,被还原,C项正确;
D. 2KMnO4![]() K2MnO4+MnO2+O2↑反应中,O元素从-2价升高到0价,被氧化,不符合题意,D项错误;
K2MnO4+MnO2+O2↑反应中,O元素从-2价升高到0价,被氧化,不符合题意,D项错误;
答案选C。

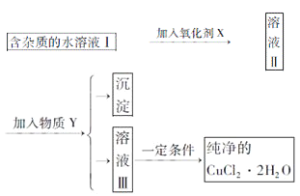
【题目】已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性,将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH的数据如下表所示。现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按图示步骤进行提纯:
氢氧化物 | 开始沉淀pH | 完全沉淀pH |
Fe(OH)2 | 6.5 | 9.7 |
Fe(OH)3 | 1.5 | 3.7 |
Cu(OH)2 | 4.2 | 6.7 |
请回答下列问题:
(1)本实验最适合的氧化剂X是__________。(选填下面的序号)
A K2Cr2O7 B NaClO C H2O2 D KMnO4
(2)物质Y是________。
(3)本实验用加碱沉淀的目的是否能达到?________________。原因是________________。
(4)除去Fe3+的化学方程式为____________________,_________________________________。
(5)加氧化剂的目的为________________________。
(6)最后能不能直接蒸发结晶得到CuCl2·2H2O晶体?________________。应如何操作________________。