题目内容
要配制浓度约为2mol·L-1NaOH溶液100mL,下面操作正确的是( )
| A.称取8gNaOH固体,放入100mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解。 |
| B.称取8gNaOH固体,放入100mL量筒中,边搅拌,便慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL。 |
| C.称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加水到刻度,盖好瓶塞,反复摇匀。 |
| D.用100mL量筒量取40mL5mol·L-1NaOH溶液,倒入250mL烧杯中,再用同一量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯。 |
D
解析试题分析:A、NaOH的物质的量为2mol,水为100mL,则配置的溶液不是100mL,浓度不是2mol?L?1,错误;B、配置100ml溶液,需要在100mL容量瓶中定容,错误;C、溶质要在烧杯中溶解,不能在容量瓶中溶解,错误;D、用该方法配置的溶液浓度为:0.04L×5mol/L÷(0.04L+0.06L)=2mol?L?1,正确。
考点:本题考查溶液的配置及计算。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室需用480mL0.5mol/L的NaOH溶液,,以下操作正确的是
| A.称取10.0gNaOH,加入500mL水 |
| B.称取10.0gNaOH,选取500mL容量瓶进行配制 |
| C.称取9.6gNaOH,选取480mL容量瓶进行配制 |
| D.称取9.6gNaOH,选取500mL容量瓶进行配制 |
Cl2、HCl的混合气体通入足量的氢氧化钠溶液,充分反应后分析产物溶液中除大量
OH? 外,还有Cl?、ClO?、ClO3?,并知这三种离子的物质的量比为9:2:1。
外,还有Cl?、ClO?、ClO3?,并知这三种离子的物质的量比为9:2:1。
试问原混合气体中Cl2与HCl体积比为( )
| A.2:5 | B.3:1  | C.5:2 | D.1:1 |
化学用语在化学学科中作用非常重要,以下有关化学用语描述正确的是:
A.Mg2+的结构图: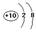 | B.Na2S的电子式: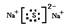 |
| C.氨气的空间结构:三角形 | D.乙烯的结构简式:(CH2)2 |
下列溶液中Cl-浓度与50 mL 1 mol·L-1 AlCl3溶液中Cl-浓度相等的是( )
| A.150 mL 1 mol·L-1的NaCl溶液 | B.75 mL 2 mol·L-1 NH4Cl溶液 |
| C.25 mL 2 mol·L-1的KCl溶液 | D.75 mL 1 mol·L-1的FeCl3溶液 |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.64g SO2含有氧原子数为NA |
| B.0.5mol/L MgCl2溶液,含有Cl-离子数为NA |
| C.标准状况下,22.4L H2O的分子数为NA |
| D.常温常压下,14g N2含有分子数为0.5NA |
下列溶液与20mL 1 mol·L_1 NaNO3溶液中NO3_物质的量浓度相等的是
| A.10 mL 1 mol·L—1 Mg(NO3)2溶液 |
| B.5 mL 0.8 mol·L—1 Al(NO3)3溶液 |
| C.10 mL 2 mol·L—1 AgNO3溶液 |
| D.10 mL 0.5 mol·L—1 Cu(NO3)2溶液 |
下列说法中正确的是( )
| A.标准状况下,22.4L水中所含的分子数约为6.02×1023个 |
| B.1 mol Cl2参加反应转移电子数一定为2 NA |
C.标准状况下,aL氧气和氮气的混合物含有的分子数约为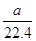 ×6.02×1023个 ×6.02×1023个 |
| D.从1 L 0.5 mol/LNaCl溶液中取出100 mL,,剩余溶液中NaCl物质的量浓度为0.45mol/L |
在MgSO4和Al2(SO4)3的混合溶液中,测得Mg2+物质的量浓度为0.1mol/L,
物质的量浓度为0.4mol/L,则混合溶液中Al3+物质的量的浓度为( )
| A.0.2mol/L | B.0.15mol/L | C.0.1mol/L | D.0.05mol/L |