题目内容
可逆反应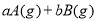

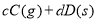
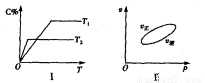
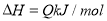 ,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图I所示,反应速率(v)与压强(p)的关系如图II所示。据图分析,以下说法正确的是( )
,反应过程中,当其他条件不变时,C在混合物中的含量与温度(T)的关系如图I所示,反应速率(v)与压强(p)的关系如图II所示。据图分析,以下说法正确的是( )
A.T1<T2,Q>0
B.增大压强,物质B的转化率增大
C.反应达平衡后,增加少量的D,平衡逆向移动
D.a+b>c+d
B
【解析】
试题分析:由图像Ⅰ可知,温度为T2时可逆反应先达到平衡状态,当其他条件不变时,温度越高,反应速率越大,达到平衡所用的时间越短,知T2>T1;温度越高,平衡时C的百分含量(C%)越小,说明平衡向左移动,当其他条件不变时,升高温度平衡向吸热方向移动,故反应的正反应为放热反应;由图像Ⅱ可知,当其他条件不变时,随着压强的增大,正速率大于逆反应速率,说明平衡向右移动,当其他条件不变时,增大压强,平衡向气体物质系数减小的方向移动,故正反应为气体物质的量减小的反应,即a+b>c。A、根据上述分析知,T2>T1,Q<0,错误;B、根据上述分析知,增大压强,平衡向右移动,物质B的转化率增大,正确;C、D为固体,反应达平衡后,增加少量的D,平衡不移动,错误;D、根据上述分析知,正反应为气体物质的量减小的反应,即a+b>c,错误。
考点:考查化学平衡图像及外界条件对化学反应速率和化学平衡的影响。

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案
相关题目