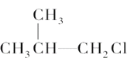题目内容
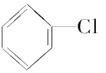
【题目】已知![]() ,
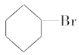
,![]() 。若在500℃和催化剂的作用下,反应在容积固定的密闭容器中进行,下列有关说法正确的是
。若在500℃和催化剂的作用下,反应在容积固定的密闭容器中进行,下列有关说法正确的是
A.达到平衡时,![]() 和
和![]() 的浓度一定相等
的浓度一定相等
B.反应体系中,当混合物的密度保持不变,反应达到平衡
C.使用催化剂、增大压强和升高温度均有利于加快反应速率
D.投入![]() 和
和![]() ,达平衡时反应放出热量为198.0 kJ
,达平衡时反应放出热量为198.0 kJ
【答案】C
【解析】
A.转化率和起始浓度未知,则反应达平衡时,SO2和SO3的浓度关系不确定,能确定的是浓度保持不变,故A错误;
B.容器的体积不变,反应体系中都是气体,气体总质量不变,根据ρ=![]() 可知反应过程中气体的密度始终不变,不能作为达平衡的标志,故B错误;
可知反应过程中气体的密度始终不变,不能作为达平衡的标志,故B错误;
C.使用催化剂、增大压强和升高温度均有利于加快反应速率,故C正确;
D.可逆反应不能完全转化,则在上述条件下,2molSO2和1molO2混合反应,放出的热量小于198.0kJ,故D错误;
答案选C。

【题目】氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解。
(1)COCl2的空间构型为______________,溴的基态原子价电子排布式为_____________。
(2)已知CsICl2不稳定,受热易分解,倾向于生成晶格能更大的物质,则它按下列_____________(填字母)式发生。
A.CsICl2====CsCl+ICl B.CsICl2====CsI+Cl2
(3)根据表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是____。
元素 | 氟 | 氯 | 溴 | 碘 |
第一电离能/ (kJ·mol-1) | 1681 | 1251 | 1140 | 1008 |
(4)下列分子既不存在“s-p”σ键,也不存在“p-p”π键的是__________(填字母)。
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-为“V”形,中心氯原子周围有4对价层电子。ClO2-中心氯原子的杂化轨道类型为______________,写出一个与CN—互为等电子体的物质的分子式:______________。
(6)钙在氧气中燃烧时得到一种钙的氧化物晶体,其结构如图所示,由此可判断钙的氧化物的化学式为__________。已知该氧化物的密度是ρg·cm-3,则晶胞内离得最近的两个钙离子的间距为_________cm(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。