题目内容
11.食品中过量的丙烯酰胺可能引起令人不安的食品安全问题.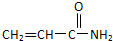
关于丙烯酰胺有下列叙述:①能使酸性KMnO4溶液褪色;②能发生加聚反应生成高分子化合物只③有4种同分异构体;④能与氢气发生加成反应.其中正确的是( )
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
分析 根据丙烯酰胺含有的官能团判断其含有的性质,丙烯酰胺中含有碳碳双键、羰基、氨基,以此来判断其含有的性质.
解答 解:①CH2=CH-CO-NH2中含有C=C以及肽键,能使酸性KMnO4溶液褪色,故①正确;
②含有C=C,能发生加聚反应生成高分子化合物,故②正确;
③丙烯酰胺的同分异构体,可书写其中的几种:H2N-CH=CH-CHO、CH≡C-CH2-O-NH2、CH≡C-O-CH2-NH2、CH3-C≡C-O-NH2、CH2=CH-CH2-NO、等等,不止四种,故③错误;
④含有C=C,能与氢气发生加成反应,故④正确;
故选D.
点评 本题考查有机物的结构和性质,题目难度不大,注意把握有机物的官能团,易错点为③,注意同分异构体的判断.

练习册系列答案
相关题目
15.用NA表示阿伏加德罗常数的值,下列有关说法错误的是( )
| A. | 1.6g氧气含有氧原子的数目为0.1NA | |
| B. | 0.5mol NH3含有的原子数目为1.5NA | |
| C. | 1mol CO2中含有的CO2分子数为NA | |
| D. | 0.5NA个臭氧(O3)分子的物质的量是0.5mol |
16.下列关于Fe(OH)3胶体的说法正确的是( )
| A. | 向Fe(OH)3胶体中加入过量的稀硫酸,产生胶体聚沉 | |
| B. | 除去Fe(OH)3胶体中混有的FeCl3溶液可选择渗析的方法 | |
| C. | 向沸腾的蒸馏水中逐滴滴加饱和FeCl3溶液,并不断搅拌即得到Fe(OH)3胶体 | |
| D. | Fe(OH)3胶体带正电荷,在通电时胶体微粒向直流电源的负极移动,这种现象称为电流 |
13.石蕊(用HIn表示)是一种常用的酸性指示剂,其电离方程式为HIn?H++In-,已知它在pH<5的溶液中呈红色,在pH>8的溶液中呈蓝色,下列判断中不正确的是( )
| A. | HIn呈红色 | B. | In-呈蓝色 | ||
| C. | 加入碱溶液后n(In-)增大 | D. | HIn呈蓝色 |
16.下列各组中,分子数目相同的是( )
| A. | 22.4 L氩气和1 mol氢气 | |
| B. | 2 g氢气和16 g氧气 | |
| C. | 同温同压下,2 L氢气和2 L水 | |
| D. | 常温常压下1 mol氧气和标准状况下2 g氢气 |
3.NA代表阿伏加德罗常数的值,以下说法正确的是( )
| A. | 2NA个HCl分子与44.8L H2和Cl2的混合气体所含的原子数目均为4NA | |
| B. | 32gCu将浓、稀硝酸分别还原为NO2和NO,浓、稀硝酸得到的电子数均为NA | |
| C. | 物质的量浓度均为1mol•L-1的NaCl和MgCl2混合溶液中,含有Cl-的数目为3NA | |
| D. | 将NA个Cl2分别通入到足量的水和NaOH溶液中,此时所转移的电子总数均为NA |
20.下列离子方程式,正确的是( )
| A. | 氢氧化铁与盐酸反应:H++OH-═H2O | |
| B. | 过量NaHSO4溶液与少量Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 铁与H2SO4反应:Fe+2H+═Fe3++H2↑ | |
| D. | CaCO3溶于稀盐酸中:CO32-+2H+═CO2↑+H2O |
1.某主族元素的离子X2+有6个电子层,最外层有2个电子,当把XO2溶于浓盐酸时,有黄绿色气体产生,则下列说法正确的是( )
| A. | X2+具有强氧化性 | B. | X的最高正价为+2价 | ||
| C. | XO2具有强氧化性 | D. | 该元素是ⅡA族 |
 三草酸合铁(Ⅲ)酸钾K3[Fe(C2O4)3]•3H2O是翠绿色单斜晶体,常温下溶解度为4.7g/100g水,难溶于乙醇,是制备负载型活性铁催化剂的主要原料.实验室制备三草酸合铁(Ⅲ)酸钾K3[Fe(C2O4)3]•3H2O的相关反应为:
三草酸合铁(Ⅲ)酸钾K3[Fe(C2O4)3]•3H2O是翠绿色单斜晶体,常温下溶解度为4.7g/100g水,难溶于乙醇,是制备负载型活性铁催化剂的主要原料.实验室制备三草酸合铁(Ⅲ)酸钾K3[Fe(C2O4)3]•3H2O的相关反应为: