题目内容
1.某主族元素的离子X2+有6个电子层,最外层有2个电子,当把XO2溶于浓盐酸时,有黄绿色气体产生,则下列说法正确的是( )| A. | X2+具有强氧化性 | B. | X的最高正价为+2价 | ||
| C. | XO2具有强氧化性 | D. | 该元素是ⅡA族 |
分析 根据离子X2+结构,推出X在周期表中的位置;根据XO2与浓盐酸发生了氧化还原反应,所以X2+还原性较差,而XO2氧化性较强.
解答 解:X2+离子最外层为2个电子,故X原子最外层有4个电子,应为ⅣA族,所以X的最高正价为+4价;XO2能氧化浓盐酸,所以X2+还原性较差,而XO2氧化性较强,
故选:C.
点评 本题考查原子结构、元素性质与元素在周期表中位置的关系,根据氧化还原反应,比较氧化性和还原性的强弱.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.食品中过量的丙烯酰胺可能引起令人不安的食品安全问题.
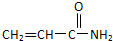
关于丙烯酰胺有下列叙述:①能使酸性KMnO4溶液褪色;②能发生加聚反应生成高分子化合物只③有4种同分异构体;④能与氢气发生加成反应.其中正确的是( )
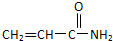
关于丙烯酰胺有下列叙述:①能使酸性KMnO4溶液褪色;②能发生加聚反应生成高分子化合物只③有4种同分异构体;④能与氢气发生加成反应.其中正确的是( )
| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
12.常见的大气污染物分为一次污染物和二次污染物,二次污染物是排入环境的一次污染物在物理化学因素或微生物作用下发生变化所生成的新污染物,如2NO+O2=2NO2,则NO2 为二次污染物,下列四种气体①SO2,②NO,③NO2,④HCl ⑤CO中能导致二次污染的是( )
| A. | 仅②⑤ | B. | 仅①②③ | C. | 仅①② | D. | 全部 |
9.下列微粒中,核外电子数相同的是①F-②Na+③Ne④K+⑤NH3( )
| A. | ①②③④ | B. | ①②④⑤ | C. | ①②③⑤ | D. | ②③④⑤ |
16.把aL含硫酸铵、硝酸铵的溶液分成两等份,一份用b mol烧碱刚好把NH4+转化为NH3,另一份与氯化钡溶液完全反应消耗c mol BaCl2.则原溶液中NO3-的浓度为( )
| A. | $\frac{2b-c}{a}$mol/L | B. | $\frac{2b-4c}{a}$mol/L | C. | $\frac{b-2c}{a}$mol/L | D. | $\frac{b-4a}{a}$mol/L |
6.化合物M结构如图所示.对化合物M的叙述正确的是( )
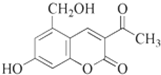

| A. | M的分子式为C12H12O5 | |
| B. | M只能与溴水发生加成反应 | |
| C. | 1mol M最多可和5mol H2发生加成反应 | |
| D. | 1molM最多可消耗3molNaOH |
10.“珍爱生命,拒绝毒品”,毒品是万恶之源.下列不属于毒品的是( )
| A. | 咖啡 | B. | 甲基苯丙胺 | C. | 可卡因 | D. | 摇头丸 |
11.下列说法正确的是( )
| A. | 摩尔质量就等于物质的相对分子质量 | |
| B. | 摩尔质量就是物质相对分子质量的6.02×1023倍 | |
| C. | HNO3的摩尔质量是63g | |
| D. | CO和N2的摩尔质量相等 |
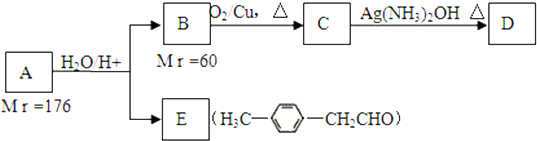
 ;; B的名称是1-丙醇;
;; B的名称是1-丙醇; 、
、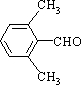 、
、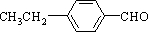 (其中一种).
(其中一种).