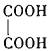题目内容
【题目】2.8g铁与100 mL稀硫酸恰好完全反应,反应前后溶液体积的变化忽略不计。求:
(1)产生的气体在标准状况下的体积。_______
(2)反应完全后,所得溶液中亚铁离子的物质的量浓度。_______
(3)反应前溶液中H+物质的量溶度。_______
【答案】1.12L 0.5mol/L 1mol/L
【解析】
(1)2.8g铁,其物质的量为![]() =0.05mol,根据反应Fe+H2SO4=FeSO4+H2↑可知,0.05molFe共生成0.05mol氢气,则产生的气体在标准状况下的体积为0.05mol×22.4L=1.12L;
=0.05mol,根据反应Fe+H2SO4=FeSO4+H2↑可知,0.05molFe共生成0.05mol氢气,则产生的气体在标准状况下的体积为0.05mol×22.4L=1.12L;
(2)2.8g铁,其物质的量为![]() =0.05mol,根据反应Fe+H2SO4=FeSO4+H2↑可知,0.05molFe共生成0.05mol FeSO4,所得溶液中亚铁离子的物质的量浓度为
=0.05mol,根据反应Fe+H2SO4=FeSO4+H2↑可知,0.05molFe共生成0.05mol FeSO4,所得溶液中亚铁离子的物质的量浓度为![]() =0.5mol/L;
=0.5mol/L;
(3)恰好完全反应,硫酸的物质的量为0.05mol,则稀硫酸的物质的量浓度为![]() =0.5mol/L,则c(H+)=2 c(H2SO4)=2×0.5 mol/L= 1mol/L;
=0.5mol/L,则c(H+)=2 c(H2SO4)=2×0.5 mol/L= 1mol/L;

【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
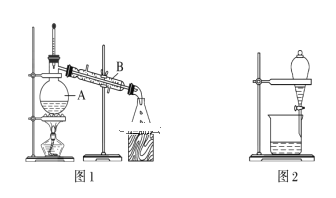

(1)装置图1中B的名称是________________,图2中漏斗的名称是________________。A中一般要加入碎瓷片,其作用是_______________________。下列关于以上实验操作说法一定正确的是_____。
A.图1实验中,加热一段时间后发现未加入碎瓷片,应马上添加,以防发生危险
B.图2实验中,应打开活塞,将有机溶剂从下端导管中放出
C.图3实验中,可以用玻璃棒在漏斗中搅拌,以加快过滤速度
D.图4实验中,当加热至有较多固体析出时,即停止加热
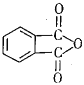
(2)现有一瓶A和B的混合液,已知它们的性质如下表。
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
A | -11.5 | 198 | 1.11 | A、B互溶,且均易溶于水和酒精 |
B | 17.9 | 290 | 1.26 |
据此分析,将A和B相互分离可选用上图中的图________________所示仪器。
【题目】足量锌与浓H2SO4充分在加热下反应生成会SO2和H2的混合气体;锌和稀硫酸反应只有H2生成。已知:Zn+2H2SO4(浓)![]() ZnSO4+2H2O+SO2↑。现有甲乙两研究小组分别实验探究:
ZnSO4+2H2O+SO2↑。现有甲乙两研究小组分别实验探究:
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL18.5mol·L-1的浓硫酸,经过一段时间反应,Zn完全溶解。

①填写仪器名称:a___________、b___________。
②研究小组认为还可能产生氢气的理由是:_____________________。
③装置D中加入的试剂是__________。
④U型管G的作用为__________。
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为__________。
⑥证明反应生成SO2和H2的实验现象是______________________________。
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是________。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是______。