题目内容
【题目】足量锌与浓H2SO4充分在加热下反应生成会SO2和H2的混合气体;锌和稀硫酸反应只有H2生成。已知:Zn+2H2SO4(浓)![]() ZnSO4+2H2O+SO2↑。现有甲乙两研究小组分别实验探究:
ZnSO4+2H2O+SO2↑。现有甲乙两研究小组分别实验探究:
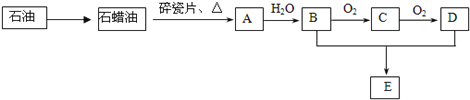
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中SO2和H2,取少量的Zn置于b中,向a中加入100mL18.5mol·L-1的浓硫酸,经过一段时间反应,Zn完全溶解。

①填写仪器名称:a___________、b___________。
②研究小组认为还可能产生氢气的理由是:_____________________。
③装置D中加入的试剂是__________。
④U型管G的作用为__________。
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为__________。
⑥证明反应生成SO2和H2的实验现象是______________________________。
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。

实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是________。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是______。
【答案】分液漏斗 圆底烧瓶 浓H2SO4逐渐变稀,Zn与稀H2SO4反应可产生H2 浓硫酸 防止空气中的水蒸气进入干燥管,干扰实验 防止倒吸 B中品红褪色,E中有红色物质生成且F中的无水硫酸铜变蓝 形成原电池反应速度快 断开K时,溶液中的c(H+)大于闭合K时溶液中的c(H+),c(H+)的影响是主要因素
【解析】
(1)①根据装置图可知仪器a是分液漏斗、b是圆底烧瓶;
②由于随反应进行,浓H2SO4逐渐变稀,Zn与稀H2SO4反应可产生H2;
③要检验氢气与氧化铜反应生成水,通入玻璃管的气体必须干燥,所以装置D中加入的试剂是干燥剂浓硫酸;
④要检验氢气与氧化铜反应生成水,要防止空气中的水蒸气进入F,所以U型管G中的碱石灰的作用是防止空气中的水蒸气进入干燥管,干扰实验;
⑤二氧化硫易溶于水,因此甲是安全瓶,可以防倒吸;
⑥SO2能使品红褪色,B中品红褪色,证明有SO2生成;H2与氧化铜反应生成水,E中有红色物质生成且F中的无水硫酸铜变蓝,证明有H2生成;
(2)①闭合K,构成铜锌原电池,反应速度快;
②断开K时的反应速率快于闭合K时的反应速率,说明从断开K开始,断开K时溶液中的c(H+)大于闭合K时溶液中的c(H+),反应后期c(H+)是影响反应速率的主要因素。

 优学名师名题系列答案
优学名师名题系列答案【题目】我国是世界上最早制得和使用金属锌的国家,一种以闪锌矿(ZnS,含有SiO2和少量FeS、CdS、PbS杂质)为原料制备金属锌的流程如图所示:

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
金属离子 | Fe3+ | Fe2+ | Zn2+ | Cd2+ |
开始沉淀的pH | 1.5 | 6.3 | 6.2 | 7.4 |
沉淀完全的pH | 2.8 | 8.3 | 8.2 | 9.4 |
回答下列问题:
(1)焙烧过程中主要反应的化学方程式为_______________________。
(2)滤渣1的主要成分除SiO2外还有___________;氧化除杂工序中ZnO的作用是____________,若不通入氧气,其后果是________________。
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式为_________________。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为______________;沉积锌后的电解液可返回_______工序继续使用。