题目内容
18.在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)?2Z(g),此反应达到平衡的标志是( )| A. | 容器内气体质量不随时间变化 | |
| B. | 容器内各物质的压强不随时间变化 | |
| C. | 容器内混合气体的密度不随时间变化 | |
| D. | 单位时间内消耗0.1mol X的同时生成0.2molZ |
分析 由X(g)+2Y(g)?2Z(g)可知,该反应前后的化学计量数之和不相等,然后根据达到平衡时,正逆反应速率相等,但不等于零,各物质的浓度不再改变来解答.
解答 解:A、反应混合物都为气体,根据质量守恒,混合气体的总质量一直不变,所以容器内气体质量不随时间变化,不能说明到达平衡状态,故A错误;
B、该反应前后的化学计量数之和不相等,容器内的压强不随时间改变,能确定达到平衡,故B正确;
C、反应混合物都为气体,根据质量守恒,混合气体的总质量不变,体积为定值,密度自始至终不变,不能说明到达平衡状态,故C错误;
D、单位时间内消耗0.1 mol X 为正速率,同时生成0.2 molZ为正速率,都是正速率不能说明达到平衡状态,故D错误;
故选B.
点评 本题考查化学平衡状态的判断,题目难度不大,做题时注意分析化学方程式的前后计量数大小的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.已知:合成氨反应(即N2+3H2═2NH3)为放热反应.反应过程中断裂1molN≡N消耗的能量为Q1kJ,断裂1molH-H消耗的能量为Q2kJ,断裂1molN-H消耗的能量为Q3kJ.下列关系式中正确的是( )
| A. | Q1+3Q2<6Q3 | B. | Q1+3Q2>2Q3 | C. | 3Q1+Q2>6Q3 | D. | Q1+3Q2<2Q3 |
9.下列各项比较中,正确的是( )
| A. | 原子核外电子数:N>O>F | B. | 元素最高化合价:Na<Mg<Al | ||
| C. | 热稳定性:HI>HCl>HF | D. | 酸性:H3PO4<H2SO4<HClO |
6.下列变化不需要破坏化学键的是( )
| A. | HCl气体溶于水 | B. | 加热HI气体使之分解 | ||
| C. | NaCl溶于水 | D. | 碘晶体受热转变成碘蒸气 |
13.医学界通过用14C标记的C60发现了一种羧酸衍生物,在特定条件下,它可以通过断裂DNA抑制艾滋病毒的繁殖.下列有关叙述中正确的是( )
| A. | 14CO2与12CO2的化学性质不同 | B. | 14CO的摩尔质量等于30g | ||
| C. | 46g 14CO2气体的体积为22.4L | D. | 14C与12C、13C互为同位素 |
3.下列第三周期元素中,非金属性最弱的是( )
| A. | 硅 | B. | 氯 | C. | 磷 | D. | 硫 |
10.下列有关实验装置或实验操作正确的是( )
 |  |  | 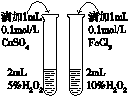 |
| 验证酸性: H2CO3>H2SiO3 | 用于分离CCl4萃取碘水后的有机层和水层 | 证明石蜡油分解生成的气体是乙烯 | 比较不同催化剂 对反应速率的影响 |
| A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
7.下列各组离子在酸性溶液中能大量共存且溶液呈无色透明的是( )
| A. | K+、Na+、SiO32-、Br- | B. | Na+、K+、CH3COO-、NO3- | ||
| C. | K+、Cl-、Fe3+、SO42- | D. | Mg2+、Al3+、Cl-、NO3- |