题目内容
现有A、B、C、D四种元素,前三种元素的离子结构都和氖原子具有相同的核外电子排布.A没有正价态的化合物;B的氢化物化学式为H2B,0.2mol的C原子能从酸中置换产生2.24LH2(S.T.P.).D的原子核中没有中子.
(1)根据以上条件,计算、推断A、B、C、D的元素名称.
(2)用电子式表示C与A,B与D,C与B(加热条件下),相互结合成的化合物,指出其化学键类型及晶体的类型.
(1)根据以上条件,计算、推断A、B、C、D的元素名称.
(2)用电子式表示C与A,B与D,C与B(加热条件下),相互结合成的化合物,指出其化学键类型及晶体的类型.
(1)A、B、C、D四种元素,前三种元素的离子结构都和氖原子具有相同的核外电子排布,A没有正价态的化合物,B的氢化物化学式为H2B,则A为F、B为O;0.2mol的C原子能从酸中置换产生2.24LH2(STP),C为金属,其化合价=
=1,则C为Na;D的原子核中没有中子,则D为H,
答:A为氟、B为氧、C为钠、D为氢.
(2)C与A的化合物为NaF,通过离子键结合而成,是离子晶体,电子式为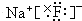 ;
;
B与D的化合物为H2O,是通过共价键形成的分子,通过分子间作力结合而成晶体,是分子晶体,电子式为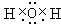 ;
;
C与B在加热条件下生成的化合物为Na2O2,既含有离子键又含有共价键,是离子晶体,电子式为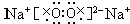 ,
,
答:NaF电子式为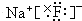 ,含有离子键,属于离子晶体;
,含有离子键,属于离子晶体;
水的电子式为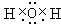 ,含有共价键,属于分子晶体;
,含有共价键,属于分子晶体;
过氧化钠电子式为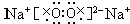 ,含有离子键、共价键,属于离子晶体.
,含有离子键、共价键,属于离子晶体.
| ||
| 0.2 |
答:A为氟、B为氧、C为钠、D为氢.
(2)C与A的化合物为NaF,通过离子键结合而成,是离子晶体,电子式为
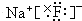 ;
;B与D的化合物为H2O,是通过共价键形成的分子,通过分子间作力结合而成晶体,是分子晶体,电子式为
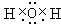 ;
;C与B在加热条件下生成的化合物为Na2O2,既含有离子键又含有共价键,是离子晶体,电子式为
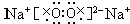 ,
,答:NaF电子式为
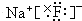 ,含有离子键,属于离子晶体;
,含有离子键,属于离子晶体;水的电子式为
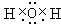 ,含有共价键,属于分子晶体;
,含有共价键,属于分子晶体;过氧化钠电子式为
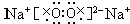 ,含有离子键、共价键,属于离子晶体.
,含有离子键、共价键,属于离子晶体.
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
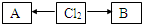 ,A、B中氯元素化合价的代数和为0,且均是共价化合物,A为强电解质,B具有漂白性,写出A→Cl2的化学反应方程式______;C与B的组成元素相同,C中氯元素的化合价为最高价,C与H2SO4相比,酸性强的是______(填化学式).
,A、B中氯元素化合价的代数和为0,且均是共价化合物,A为强电解质,B具有漂白性,写出A→Cl2的化学反应方程式______;C与B的组成元素相同,C中氯元素的化合价为最高价,C与H2SO4相比,酸性强的是______(填化学式).
