题目内容
【题目】下列有关离子反应的说法正确的是( )
选项 | 离子方程式 | 评价 |
A | 将2molCl2通入到含1mol FeI2的溶液中:2Fe2++2I-+2Cl2= 2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ | 正确;阳极氯离子放电,阴极氢离子放电 |
C | 向AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O=A1O2一 + 4NH4++ 2H2O | 正确;氨水过量,氢氧化铝能溶于过量的碱 |
D | 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O | 错误;电荷不守恒,生成物中应有亚铁离子 |
A.AB.BC.CD.D
【答案】D
【解析】
A选项,将2molCl2通入到含1mol FeI2的溶液,2mol I-先被1mol氯气氧化,再是1mol Fe2+被0.5mol氯气氧化,氯气过量,因此离子方程式为2Fe2++4I-+3Cl2= 2Fe3++6Cl-+2I2,故A错误;
B选项,用惰性电极电解饱和氯化钠溶液:2Cl- + 2H2O![]() H2↑ + Cl2↑ + 2OH-,阳极氯离子放电,阴极氢离子放电,但总反应中氢离子来自于水,不拆,故B错误;
H2↑ + Cl2↑ + 2OH-,阳极氯离子放电,阴极氢离子放电,但总反应中氢离子来自于水,不拆,故B错误;
C选项,向AlCl3溶液中加入过量的浓氨水,生成氢氧化铝沉淀和氯化铵,因此离子方程式为:Al3++3NH3·H2O=A1(OH)3↓ + 3NH4+,故C错误;
D选项,将磁性氧化铁溶于盐酸生成氯化亚铁、氯化铁和水,其离子方程式为Fe3O4 + 8H+ = 2Fe3+ + Fe2+ + 4H2O,因此判断正确,故D正确。
综上所述,答案为D。

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案【题目】实验室模拟工业生产食品香精菠萝酯(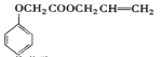 )的简易流程如下:
)的简易流程如下:
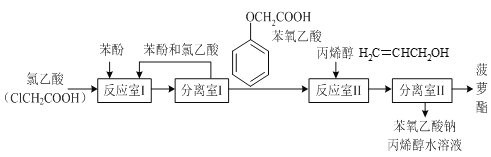
有关物质的熔、沸点如表:
苯酚 | 氯乙酸 | 苯氧乙酸 | |
熔点/℃ | 43 | 62 | 99 |
沸点/℃ | 181.9 | 189 | 285 |
试回答下列问题:
(1)反应室I中反应的最佳温度是104℃,为较好地控制温度在102℃~106℃之间,加热时可选用___(选填字母)。
A.火炉直接加热 B.水浴加热 C.油浴加热
(2)分离室I采取的操作名称是___。
(3)反应室I中发生反应的化学方程式是___。
(4)分离室II的操作为:①用NaHCO3溶液洗涤后分液;②有机层用水洗涤后分液;洗涤时不能用NaOH溶液代替NaHCO3溶液,其原因是___(用化学方程式表示)。
