题目内容
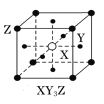
【题目】25℃时Ksp(FeS)=6.3×10-18,Ksp(CuS)=6.3×10-36,Ksp(MnS)=2.5×10-13,常温下三种物质在水中的沉淀溶解平衡线如图所示(X表示Fe、Cu、Mn)。下列说法正确的是( )

A.曲线Ⅰ表示CuS的溶解平衡曲线
B.Ag2S在a点溶液中的溶解度小于在b点溶液中的溶解度
C.c点与d点溶液中S2-的物质的量浓度相等
D.向含有XS固体的d点溶液中滴加稀硫酸至过量可使固体逐渐溶解
【答案】B
【解析】
A. XS的饱和溶液中,c(X2+)=![]() ,Ksp越大,c(X2+)越大;
,Ksp越大,c(X2+)越大;
B. Ag2S溶解时存在溶解平衡,S2-对Ag2S的溶解有抑制作用;
C. 由图象可知,c点溶液中S2-的浓度大于d点溶液中S2-的浓度;
D. d点溶液中c(X2+)= c(S2-)=![]() 最小,应为CuS的饱和溶液,再结合CuS的特性进行分析。
最小,应为CuS的饱和溶液,再结合CuS的特性进行分析。
A. XS的饱和溶液中,c(X2+)=![]() ,根据溶度积的大小可知,曲线I、II、III分别为MnS、FeS、CuS的溶解平衡曲线,A项错误;
,根据溶度积的大小可知,曲线I、II、III分别为MnS、FeS、CuS的溶解平衡曲线,A项错误;
B. Ag2S溶解时存在溶解平衡,S2-对Ag2S的溶解有抑制作用,a点溶液中S2-的浓度大于b点溶液中S2-的浓度,因此Ag2S在a点溶液中的溶解度小于在b点溶液中的溶解度,B项正确;
C. 由图象可知,c点溶液中S2-的浓度大于d点溶液中S2-的浓度,C项错误;
D.CuS难溶于稀硫酸,因此向含有XS固体的饱和溶液中滴加稀硫酸至过量不能使固体逐渐溶解,D项错误;
答案选B。

【题目】高炉炼铁过程中发生反应:![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如表,下列说法正确的是( )
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如表,下列说法正确的是( )
温度 | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
A.ΔH>0
B.1000℃时,在固定体积的密闭容器中,某时刻测得上述体系中,CO、CO2的物质的量分别为0.5 mol、1.8 mol,此时反应向正反应方向进行
C.其他条件不变,向平衡体系充入CO2气体,K值减小
D.其他条件不变,升高温度,可以提高CO的平衡转化率
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将SO2气体通入Ba(NO3)2溶液 | 有白色沉淀 | SO2中混有SO3 |
B | 向NaAlO2溶液中持续通入气体Y | 先出现白色沉淀,最终沉淀又溶解 | Y可能是CO2气体 |
C | AgCl悬浊液中滴入少量Na2S溶液 | 沉淀变黑色 | Ksp(Ag2S)>Ksp(AgCl) |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在平衡: I3- |
A. A B. B C. C D. D
【题目】下列有关离子反应的说法正确的是( )
选项 | 离子方程式 | 评价 |
A | 将2molCl2通入到含1mol FeI2的溶液中:2Fe2++2I-+2Cl2= 2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | 用惰性电极电解饱和氯化钠溶液:2Cl-+2H+ | 正确;阳极氯离子放电,阴极氢离子放电 |
C | 向AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O=A1O2一 + 4NH4++ 2H2O | 正确;氨水过量,氢氧化铝能溶于过量的碱 |
D | 将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O | 错误;电荷不守恒,生成物中应有亚铁离子 |
A.AB.BC.CD.D