题目内容
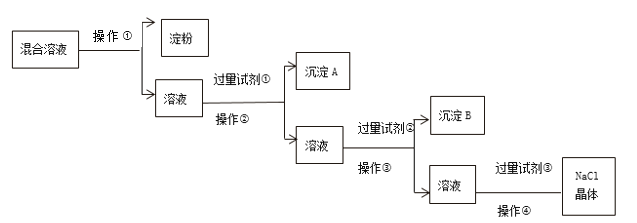
【题目】现有淀粉、NaCl、Na2SO4、CaCl2的混合溶液,选择适当的试剂和方法从中提纯出NaC1晶体,相应的实验过程如下:
(1)操作①是利用胶体不能通过___________而把淀粉胶体和溶液进行分离。
(2)写出上述实验过程中所用试剂的化学式:试剂①____________;试剂③___________。
(3)判断试剂①已过量的操作是______________________。
(4)操作④的名称是____________。
(5)试剂的作用(用离子方程式表示):__________________________________。
【答案】半透膜 BaCl2 HCl 静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量 重结晶 Ba2++CO32-=BaCO3↓
【解析】
胶体不能透过半透膜,操作①为渗析,除去Na2SO4、CaCl2,可分别加入BaCl2、Na2CO3,除去粗盐中含有的Ca2+、SO42-可溶性杂质的方法:加入过量BaCl2,去除硫酸根离子;再加入过量Na2CO3(去除钙离子),则试剂①为BaCl2,操作②为过滤,沉淀A为硫酸钡,试剂②为Na2CO3,操作③为过滤,沉淀B为碳酸钙和碳酸钡,试剂③为盐酸,加入盐酸可除去过量的Na2CO3,最后蒸发结晶可得到NaCl晶体.
(1)淀粉为胶体,粒子直径较大,不能透过半透膜,所以可以把淀粉胶体和溶液进行分离,操作①是利用胶体不能通过半透膜而把淀粉胶体和溶液进行分离。
(2)写出上述实验过程中所用试剂的化学式:试剂①BaCl2;试剂③HCl。
(3)判断试剂①已过量的操作是:静置,向上层清液中滴加少量氯化钡溶液,没有白色沉淀产生,说明氯化钡溶液已过量。
(4)操作④的名称是重结晶。
(5)试剂的作用为Na2CO3,是用来除去溶液中的钡离子的,(用离子方程式表示):Ba2++CO32-=BaCO3↓

 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案