题目内容
【题目】烃A在一定条件下可以按图进行转化: 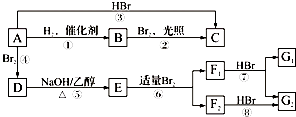 已知D为
已知D为 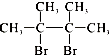 ,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体.据此作答:
,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,G1和G2分别互为同分异构体.据此作答:
(1)框图中属于取代反应的是(填序号);B完全燃烧后生成的CO2和水的质量比为 .
(2)A的结构简式是;G1的结构简式是 .
(3)写出E在一定条件下生成高聚物的化学方程式:
(4)已知B可在碱性条件下和O2构建成燃料电池,写出负极的电极反应式 .
【答案】
(1)②;44:21
(2)(CH3)2C=C(CH3)2;![]() ;
;
(3)![]()
(4)C6H14﹣38e﹣+50 OH﹣=6CO ![]() +32H2O
+32H2O
【解析】解:由D的结构可知A为(CH3)2C=C(CH3)2 , E为CH2=C(CH3)C(CH3)=CH2 , 则B为(CH3)2CHCH(CH3)2 , C为(CH3)2CHCBr(CH3)2 , CH2=C(CH3)C(CH3)=CH2可与溴发生1,2﹣加成或﹣1,4加成,F1和F2互为同分异构体,加成HBr时F1有两种加成产物,F2只有一种加成产物,则F1为CH2BrCBr(CH3)C(CH3)=CH2 , F2为CH2BrC(CH3)=C(CH3)CH2Br,且F1、F2都可生成G2 , G1为 ![]() ,G2为
,G2为 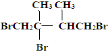 .(1)反应①为加成反应,②为取代反应,③为加成反应,④为加成反应,⑤为消去反应,⑥为加成反应,⑦为加成反应,⑧为加成反应; B为(CH3)2CHCH(CH3)2 , 由元素守恒可知生成的CO2和水的质量比为6mol×44g/mol:
.(1)反应①为加成反应,②为取代反应,③为加成反应,④为加成反应,⑤为消去反应,⑥为加成反应,⑦为加成反应,⑧为加成反应; B为(CH3)2CHCH(CH3)2 , 由元素守恒可知生成的CO2和水的质量比为6mol×44g/mol: ![]() ×18g/mol=44:21,所以答案是:②;44:21;(2)A的结构简式是 (CH3)2C=C(CH3)2;G1的结构简式是
×18g/mol=44:21,所以答案是:②;44:21;(2)A的结构简式是 (CH3)2C=C(CH3)2;G1的结构简式是 ![]() ,所以答案是:(CH3)2C=C(CH3)2;
,所以答案是:(CH3)2C=C(CH3)2; ![]() ;(3)E在一定条件下生成高聚物的化学方程式:
;(3)E在一定条件下生成高聚物的化学方程式: ![]() ,
,
所以答案是: ![]() ;(4)负极发生氧化反应,(CH3)2CHCH(CH3)2在负极失去电子,进行条件下生成碳酸根与水,负极的电极反应式:C6H14﹣38e﹣+50 OH﹣=6CO32﹣+32H2O,所以答案是:C6H14﹣38e﹣+50 OH﹣=6CO32﹣+32H2O.
;(4)负极发生氧化反应,(CH3)2CHCH(CH3)2在负极失去电子,进行条件下生成碳酸根与水,负极的电极反应式:C6H14﹣38e﹣+50 OH﹣=6CO32﹣+32H2O,所以答案是:C6H14﹣38e﹣+50 OH﹣=6CO32﹣+32H2O.

 名校练考卷期末冲刺卷系列答案
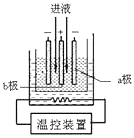
名校练考卷期末冲刺卷系列答案【题目】实验室制备1,2﹣二溴乙烷的反应原理如下:CH3CH2OH ![]() CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图:
CH2=CH2 , CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2﹣二溴乙烷的装置如图: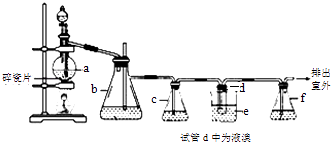
有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | ﹣130 | 9 | ﹣116 |
回答下列问题:
(1)在装置c中应加入(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水 ②浓硫酸 ③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是 .
(3)将二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在水的(填“上”或“下”)层.
(4)若产物中有少量未反应的Br2 , 最好用(填正确选项前的序号)洗涤除去.
①水 ②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(5)反应过程中需用冷水冷却(装置e),其主要目的是;但不用冰水进行过度冷却,原因是:
(6)以1,2﹣二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2﹣二溴乙烷通过(①)反应制得(②),②通过( ③)反应制得氯乙烯,由氯乙烯制得聚氯乙烯.
①(填反应类型)②(填该物质的电子式)③(填反应类型)写出第一步的化学方程式 .
【题目】古诗词是古人为我们留下的宝贵精神财富。下列诗句中只涉及物理变化的是( )
A.野火烧不尽,春风吹又生B.春蚕到死丝方尽,蜡炬成灰泪始干
C.只要功夫深,铁杵磨成针D.爆竹声中一岁除,春风送暖入屠苏
【题目】能源是人类生存和发展的重要支柱,研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义,已知下列热化学方程式 ①H2(g)+ ![]() O2(g)=H2O(g)△H=﹣242kJ/mol;
O2(g)=H2O(g)△H=﹣242kJ/mol;
②2H2(g)+O2(g)=2H2O(l)△H=﹣572kJ/mol;
③C(s)+ ![]() O2(g)=CO(g)△H=﹣110.5kJ/moL;
O2(g)=CO(g)△H=﹣110.5kJ/moL;
④C(s)+O2(g)=CO2(g)△H=﹣393.5kJ/moL;
⑤CO2(g)+2H2O(g)=CH4(g)+2O2(g)△H=+802kJ/moL
化学键 | O=O | C﹣C | H﹣H | O﹣O | C﹣O | O﹣H | C﹣H |
键能kJ/mol | 497 | 348 | 436 | 142 | 351 | 463 | 414 |
回答下列问题
(1)写出能表示H2燃烧热的热化学方程式:
(2)计算C(s)+H2O(g)H2(g)+CO(g)△H=kJ/moL;
(3)估算出C=O键能为kJ/moL.
(4)CH4的燃烧热△H=﹣kJ/moL.
(5)25℃、101kPa下,某燃具中CH4的燃烧效率是90%(注:相当于10%的CH4未燃烧),水壶的热量利用率是70%,则用此燃具和水壶,烧开1L水所需要的CH4的物质的量为mol[保留到小数点后2位;c (H2O)=4.2J/(g℃)].