题目内容
13.W、X、Y、Z为短周期内除稀有气体元素外的四种元素,它们的原子序数依次增大,其中W是原子序数最小的元素,只有Y为金属元素.Y 和W的最外层电子数相等.Y、Z两元素原子的质子数之和为W、X两元素原子质子数之和的3倍.请回答下列问题.①写出下列元素的元素符号:WH,XO,YNa,ZS.
②W2Z是由共价(填“离子”或“共价”)键组成的分子,其电子式为
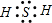 .
.③由X、Y、Z组成的物质是由离子键和共价键组成的离子化合物.(填“离子”或“共价”)
分析 W是原子序数最小的元素,则W为H元素;Y和W的最外层电子数相等,则W和Y同主族,结合原子序数大小可知Y为Na元素;
Y的质子数是11,Z一定大于Y,也就是12以上,故Y和Z的和能被3整除的数有:24、27,故Z质子数为:24-11=13,或27-11=16,W的质子数是1,X的质子数有可能是7或8,故W、Z、Y、Z分别为:1,7,11,13(铝为另一种金属)不成立,或1,8,11,16 成立,所以W、X、Y、Z分别为H、O、Na、S,据此进行解答.
解答 解:①W是原子序数最小的元素,则W为H元素;Y和W的最外层电子数相等,则W和Y同主族,结合原子序数大小可知Y为Na元素;
Y的质子数是11,Z一定大于Y,也就是12以上,故Y和Z的和能被3整除的数有:24、27,故Z质子数为:24-11=13,或27-11=16,W的质子数是1,X的质子数有可能是7或8,故W、Z、Y、Z分别为:1,7,11,13(铝为另一种金属)不成立,或1,8,11,16 成立,所以W、X、Y、Z分别为H、O、Na、S,
故答案为:H;O;Na;S;
②W2Z为H2S,硫化氢属于共价化合物,只含有共价键;硫化氢的电子式为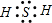 ,故答案为:共价;
,故答案为:共价;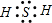 ;
;
③由X、Y、Z组成的物质为亚硫酸钠或硫酸钠,二者都是由离子键和共价键组成的离子化合物,故答案为:离子;共价;离子.
点评 本题考查了位置结构与性质关系的应用,题目难度不大,试题侧重基础知识的考查,正确推断各元素名称为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系.

练习册系列答案
相关题目
4.下列说法中正确的是( )
| A. | 完全由非金属组成的化合物不一定是共价化合物 | |
| B. | 构成分子晶体的粒子一定含有共价键 | |
| C. | 分子晶体的熔点一定比金属晶体的熔点低 | |
| D. | 含有金属离子的晶体一定是离子晶体 |
1.a、b、c、d均为短周期元素,它们在周期表中的位置如图所示.下列说法正确的是( )
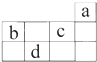

| A. | a原子的最外电子层上有8个电子 | |
| B. | c的最高价氧化物对应水化物为强酸 | |
| C. | d的原子半径比c的原子半径大 | |
| D. | b的气态氢化物比c的气态氢化物稳定 |
8.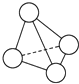 N4的分子结构类似白磷分子, 它的结构如图所示,已知断裂1mol N-N键需要吸收167kJ热量,生成1mol N≡N键需放出942kJ热量.根据以上信息和数据,下列说法中正确的是( )
N4的分子结构类似白磷分子, 它的结构如图所示,已知断裂1mol N-N键需要吸收167kJ热量,生成1mol N≡N键需放出942kJ热量.根据以上信息和数据,下列说法中正确的是( )
 N4的分子结构类似白磷分子, 它的结构如图所示,已知断裂1mol N-N键需要吸收167kJ热量,生成1mol N≡N键需放出942kJ热量.根据以上信息和数据,下列说法中正确的是( )
N4的分子结构类似白磷分子, 它的结构如图所示,已知断裂1mol N-N键需要吸收167kJ热量,生成1mol N≡N键需放出942kJ热量.根据以上信息和数据,下列说法中正确的是( )| A. | 1 mol N4气体转变为N2将放出775 kJ热量 | |
| B. | 1 mol N4气体转变为N2将放出882 kJ热量 | |
| C. | 1 mol N4气体转变为N2将吸收775 kJ热量 | |
| D. | 1 mol N4气体转变为N2将吸收882 kJ热量 |
18.已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,根据化学方程式:N2+3H2$?_{高温高压}^{催化剂}$2NH3,1mol N2与足量H2反应放出的热量为92.4kJ•mol-1,那么N≡N键的键能是( )
| A. | 431kJ•mol-1 | B. | 945.6kJ•mol-1 | C. | 649kJ•mol-1 | D. | 896kJ•mol-1 |
5.下列实验操作或叙述正确的是( )
| A. | 通过导电实验证明氢氧化铁胶体带正电 | |
| B. | 除去苯中溶有的少量乙醇,加入水,振荡,然后分液 | |
| C. | 进行蒸馏操作时.应用温度计准确测量沸腾液体的温度 | |
| D. | 从海带中提取碘时用到的药品有双氧水和NaOH溶液 |
