题目内容
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)具有良好的热稳定性、耐热性、电绝缘性,是目前用量最大的热稳定剂,工业上利用铅废渣(主要含PbSO4、 PbCl2、 SiO2)制取三盐基硫酸铅及PbO2工艺流程如下:

已知:①“浸出”过程发生的反应:PbSO4(s)+2Cl-(aq)![]() PbCl2+SO42-(aq)和
PbCl2+SO42-(aq)和
PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0,
PbCl42-(aq) △H>0,
②Ksp(PbCl2)=1.7×10-5 Ksp(PbSO4)=2.5×10-8
回答下列问题:
(1)铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和___________。
(2)“操作1”通过多步操作得到PbCl2,分别为___________、___________、过滤、洗涤。
(3)“转化”后得到PbSO4,当c(Cl-)=0.100mol/L时,c(SO42-)=___________(结果保留一位小数);“转化”时需要升高体系温度,其原因是_________________________________。
(4)写出合成三盐基硫酸铅的化学方程式_________________________________。
(5)氨水络合后铅的存在形态是[ Pb(OH)SO4]-,写出“氧化”发生的离子反应方程式__________________________________________________________________。
(6)一种新型的铅锂电池的充放电示意图如下,写出放电时的正极反应式___________。

【答案】SiO2 蒸发浓缩 冷却结晶 1.5×10-5mol/L 升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)![]() PbSO4(s)+2HCl(aq)向右移动 4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O [Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O Li1-xMn2O4+xe-+xLi+=LiMn2O4
PbSO4(s)+2HCl(aq)向右移动 4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O [Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O Li1-xMn2O4+xe-+xLi+=LiMn2O4
【解析】
铅废渣(主要含PbSO4、 PbCl2、 SiO2)加入CaCl2 、NaCl溶液,“浸出”过程发生的反应:PbSO4(s)+2Cl-(aq)![]() PbCl2+SO42-(aq)和PbCl2(s)+2Cl-(aq)
PbCl2+SO42-(aq)和PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2,“操作1”通过多步操作得到PbCl2,分别为蒸发浓缩、冷却结晶、过滤、洗涤。加入硫酸“转化”后得到PbSO4,溶液Ⅱ为HCl,加入NaOH合成三盐基硫酸铅,反应为:4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O,加NH3·H2O络合后溶解生成[ Pb(OH)SO4]-,加入(NH4)2S2O82-发生[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O,得PbO2。
PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2,“操作1”通过多步操作得到PbCl2,分别为蒸发浓缩、冷却结晶、过滤、洗涤。加入硫酸“转化”后得到PbSO4,溶液Ⅱ为HCl,加入NaOH合成三盐基硫酸铅,反应为:4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O,加NH3·H2O络合后溶解生成[ Pb(OH)SO4]-,加入(NH4)2S2O82-发生[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O,得PbO2。
(1)铅废渣(主要含PbSO4、 PbCl2、 SiO2)加入CaCl2 、NaCl溶液,“浸出”过程发生的反应:PbSO4(s)+2Cl-(aq)![]() PbCl2(s)+SO42-(aq)和PbCl2(s)+2Cl-(aq)
PbCl2(s)+SO42-(aq)和PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2;
PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2;
(2)“操作1”分别经过蒸发浓缩、冷却结晶、过滤、洗涤得到PbCl2晶体。
(3)“转化”后得到PbSO4,PbSO4(s)+2Cl-(aq)![]() PbCl2(s)+SO42-(aq),当c(Cl-)=0.100mol/L时,c(SO42-)=c2(Cl-)Ksp(PbSO4)/Ksp(PbCl2)=0.1002×2.5×10-8/1.7×10-5=1.5×10-5;“转化”时需要升高体系温度,其原因是升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)
PbCl2(s)+SO42-(aq),当c(Cl-)=0.100mol/L时,c(SO42-)=c2(Cl-)Ksp(PbSO4)/Ksp(PbCl2)=0.1002×2.5×10-8/1.7×10-5=1.5×10-5;“转化”时需要升高体系温度,其原因是升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)![]() PbSO4(s)+2HCl(aq)向右移动。
PbSO4(s)+2HCl(aq)向右移动。
(4)已知三盐基硫酸铅(3PbO·PbSO4·H2O),反应物为PbSO4和NaOH,合成三盐基硫酸铅的化学方程式4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O。
(5)3PbO·PbSO4·H2O氨水络合后铅的存在形态是[ Pb(OH)SO4/span>]-,+2价铅氧化成+4价,“氧化”发生的离子反应方程式[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O。
(6)新型的铅锂电池放电时正极发生还原反应,正极反应式Li1-xMn2O4+xe-+xLi+=LiMn2O4。

【题目】CO2是主要的温室气体,也是一种工业原料。回收利用CO2有利于缓解温室效应带来的环境问题。
(1)我国科学家通过采用一种新型复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油。
已知:2H2 (g)+O2 (g) =2H2O(l) ΔH = -571.6 kJ/mol
2C8H18(l)+25O2(g) =16CO2(g)+18H2O(l) ΔH = -11036 kJ/mol

25℃、101kPa条件下,CO2与H2反应生成辛烷(以C8H18表示)和液态水的热化学方程式是_________。
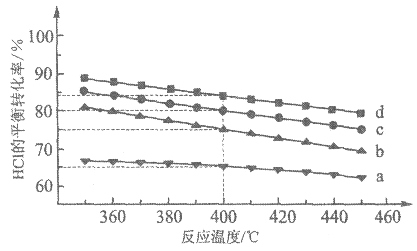
(2)CO2催化加氢合成乙醇的反应原理是:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=![]() 。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
(3)在Cu/ZnO催化剂存在下,将CO2与H2混合可合成甲醇,同时发生以下两个平行反应:
反应Ⅰ CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
反应Ⅱ CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
控制一定的CO2和H2初始投料比,在相同压强下,经过相同反应时间测得如下实验数据(其中“甲醇选择性”是指转化的CO2中生成甲醇的百分比):
实验序号 | T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
实验1 | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
实验2 | 543 | Cu/ZnO纳米片 | 10.9 | 72.7 |
实验3 | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
实验4 | 553 | Cu/ZnO纳米片 | 12.0 | 71.6 |
①对比实验1和实验3可发现:同样催化剂条件下,温度升高,CO2转化率升高, 而甲醇的选择性却降低,请解释甲醇选择性降低的可能原因_______________;
②对比实验1和实验 2可发现:在同样温度下,采用Cu/ZnO纳米片使CO2转化率降低, 而甲醇的选择性却提高,请解释甲醇的选择性提高的可能原因____________。
③有利于提高CO2转化为CH3OH平衡转化率的措施有_______。
a.使用Cu/ZnO纳米棒做催化剂
b.使用Cu/ZnO纳米片做催化剂
c.降低反应温度
d.投料比不变,增加反应物的浓度
e.增大![]() 的初始投料比
的初始投料比
(4)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2,电解,在阴极可制得低密度聚乙烯![]() (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是_____________。
②工业上生产1.4×104 kg 的LDPE,理论上需要标准状况下______L 的CO2。