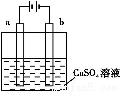
题目内容
设NA代表阿伏加德罗常数,下列叙述正确的是( )
A.标准状况下2.24 L H2O中,分子数为0.1 NA
B.将1 mol Cl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2NA
C.常温常压下16 g O2和O3混合气体中,氧原子数为NA
D.7.8 g Na2O2与足量水反应,转移电子数为0.2NA
C
【解析】A项,标准状况下,水为液体;B项,Cl2和H2O反应是可逆反应,2N(Cl2)+N(HClO)+N(Cl-)+N(ClO-)=2NA;D项,Na2O2与水反应,Na2O2既是氧化剂,又是还原剂,7.8 g Na2O2与水反应,应转移0.1NA电子。

请参考题中图表,已知E1=134 kJ·mol-1、E2=368 kJ·mol-1,根据要求回答问题:
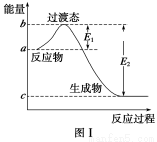
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”、“减小”或“不变”,下同),ΔH的变化是________。请写出NO2和CO反应的热化学方程式:________________________________。
(2)甲醇质子交换膜燃料电池中将甲醇蒸汽转化为氢气的两种反应的热化学方程式如下:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1
②CH3OH(g)+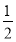 O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,则甲醇蒸汽燃烧为液态水的热化学方程式为______________________。
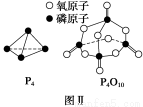
(3)如表所示是部分化学键的键能参数:
化学键 | P—P | P—O | O=O | P=O |
键能/kJ·mol-1 | a | b | c | x |
已知白磷的燃烧热为d kJ·mol-1,白磷及其完全燃烧的产物的结构如图Ⅱ所示,则表中x=________ kJ·mol-1(用含a、b、c、d的代表数式表示)。