��Ŀ����
(1)ijС��Ϊ�о��绯ѧԭ��,�����ͼװ��,����������ȷ���� ��
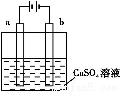
A.��a��bΪʯī,ͨ���a�缫�Ϸ����ķ�ӦΪCu2++2e-=Cu
B.��a��bΪʯī,ͨ�������̪,a�缫������Һ�ʺ�ɫ
C.��aΪͭ,bΪ��,ͨ���Cu2+��a�缫�ƶ�
D.��aΪ��ͭ,bΪ��ͭ,ͨ���b�缫��������
(2)���ʱ,�Ƽ����Դ�� �����ӡ���ѧ�Ƶ�ԭ�������û�ѧ��Ӧ���ɽ������ʳ����ڶƼ������γɶƲ㡣
������ͭ�ν��л�ѧ��ͭ,Ӧѡ�� (�����������ԭ����)��֮��Ӧ��
��ij��ѧ��ͭ�ķ�Ӧ�������ҺpH�仯��ͼ��ʾ���ö�ͭ������,��ҺpH������12.5���ҡ���ͼ����Ϣ,����ʹ��Ӧֹͣ�ķ���: ��

(1)D
(2)�� �ٻ�ԭ�� �ڵ�����ҺpHС��9
��������(1)a��bΪʯī,���CuSO4��Һ,a�缫������,�缫��Ӧ:4OH--4e-=2H2O+O2��,Aѡ���;����a�缫��OH-�ŵ�,���H+Ũ������,��Һ������,�����̪,��Һ����ɫ,Bѡ���;��aΪͭ,��a�缫ͭʧ���Ӷ��ܽ�,Cu-2e-=Cu2+,b�缫��Cu2++2e-=Cu,����Cu2+��b���ƶ�,Cѡ���;aΪ��ͭ,���ܽ�,bΪ��ͭ,��ͭ��������������,Dѡ����ȷ��
(2)���ʱ,�Ƽ����Դ�ĸ�������,��Һ�еĶƲ�������ӵõ������ڶƼ���������
�ٻ�ѧ�Ƶ�ԭ�����������û���Ӧ���Ʋ�������Ӵ���Һ���û�����,��ͭ�����û���ͭͨ��ѡ��Fe�Ȼ�ԭ����
����ͼ�ɿ�����ҺpH����9ʱ,�û�ѧ�Ƶķ�Ӧ����Ϊ0,��˿ɵ���pH��С��9����ʹ��Ӧֹͣ��

Ϊ̽����ҵ����������ͭ�Ͻ���ϵ�������,��ͬѧ��Ƶ�ʵ�鷽������:

��ش�:
(1)�������õ��IJ��������� ��
(2)д����Ӧ�ٵĻ�ѧ����ʽ: ,��Ӧ�ڵ����ӷ�Ӧ����ʽ: ��
(3)���ʵ�鷽��,�����ҺD�к��еĽ�������(�Լ���ѡ) ��
(4)������E�м���ϡ������Լ�Y�Ƶ���������һ����ɫ��ѧ����,�Լ�YΪ��ɫҺ��,��Ӧ�ܵ��ܻ�ѧ����ʽ�� ��
(5)��ͬѧ�ڼ�ͬѧ�����Ļ��������������B���Ʊ�FeCl3��6H2O����,�������еμ�����ʱ,���ַ�Ӧ���ʱ�ͬŨ�������봿���۷�ӦҪ��,��ԭ���� ��
�������Ȼ�����Һ�ü���Ũ�������½ᾧ���Ƶ�FeCl3��6H2O ����,������ֱ�������ᾧ�ķ������Ƶþ���������� ��
(6)������B�ľ��Ȼ����ƽ���ֳ��ĵȷ�,�ֱ����ͬŨ�ȵ�ϡ����,��ַ�Ӧ��,�ڱ�״��������NO�������ʣ��������������±�(������Ļ�ԭ����ֻ��NO)��
ʵ���� | �� | �� | �� | �� |
ϡ�������(mL) | 100 | 200 | 300 | 400 |
ʣ���������(g) | 9.0 | 4.8 | 0 | 0 |
NO���(L) | 1.12 | 2.24 | 3.36 | V |
�������Ũ��Ϊ ;�����ܽ�ͭ������Ϊ ;����V= ��
������ĿҪ��ش��������⡣
(1)������,Ũ�Ⱦ�Ϊ0.1 mol��L-1������������Һ��pH�����ʾ��
���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
����������Һ�е������ӽ��H+������ǿ���� ��
�ڸ��ݱ�������,Ũ�Ⱦ�Ϊ0.01 mol��L-1�������������ʵ���Һ��,������ǿ���� (����ĸ���,��ͬ);������Һ�ֱ�ϡ��100��,pH�仯��С���� ��
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
�۸����ϱ�����,�����ж����з�Ӧ���ܳ������� ��
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+NaClO=NaHCO3+HClO
D.CO2+H2O+2C6H5Ona=Na2CO3+2C6H5OH
��Ҫ������ˮ��HClO��Ũ��,������ˮ�м���������̼��������Һ,��Ӧ�����ӷ���ʽΪ ��
(2)��֪������Cu(OH)2��Ksp=2��10-20����֪������ijCuSO4��Һ��c(Cu2+)=0.02 mol��L-1,���Ҫ����Cu(OH)2 ����,��Ӧ������Һ��pH���� ��