题目内容
乙烯(C2H4)和乙烷(C2H6)的混合气体共amol,与bmolO2共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45gH2O,试求:
(1)当a=1时,乙烯和乙烷的物质的量之比n(C2H4):n(C2H6)= 。
(2)当a=1,且反应后CO和CO2的混合气体的物质的量为反应前O2的2/3时,b= ,得到的CO和CO2的物质的量之比n(CO)∶n(CO2)= 。
(3)a的取值范围是 。
练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案
相关题目
4.高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理为:2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O,下列说法正确的是( )
| A. | ClO-做还原剂 | |
| B. | 制备1molK2FeO4时转移3mol 电子 | |
| C. | 高铁酸钾中铁的化合价为+7 | |
| D. | Fe(OH)3在反应中被还原,发生还原反应 |
2.在V L密闭容器中投入足量的硫酸钙和a mol CO进行可逆反应:CaSO4(s)+4CO(g)?CaS(s)+4CO2(g)△H.在一定温度下达到平衡,测得平衡体系中CO,CO2的体积比为1:1,下列说法不正确的是( )
| A. | 若该反应在较低温度下能自发进行,则△H<0 | |
| B. | 在该温度下上述反应的平衡常数K=4 | |
| C. | 达到平衡时生成了0.125amol CaS | |
| D. | 向上述体系中加入石灰石,能提高CO的转化率 |
(1)若某药品质量约为32.0g, 托盘天平准确称其质量,若用↓表示在右盘放上砝码,用↑表示将砝码取下,在下列表格的空格内,用↓和↑表示相应砝码的放上或取下.
50g | 20g | 20g | 10g | 5g |
(2)配制500mL 0.1mol.L-1 Na2CO3溶液,图中操作②中应该填写的数据为__________,实验操作的先后顺序为________________ (填编号)。
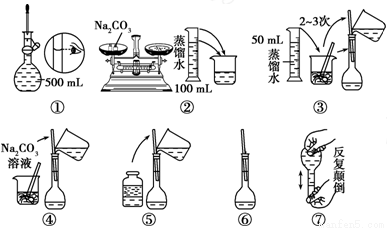
(3)在配制一定物质的量浓度的溶液时,用“偏高、偏低、无影响”表示下列操作对所配溶液浓度的影响。
①用量筒取液态溶质,读数时,俯视量筒,所配制溶液的浓度___________
②将量取液态溶质的量筒用水洗涤,洗涤液倒入容量瓶,所配制溶液的浓度___________
③定容摇匀后,有少量溶液外流,对所配制溶液的浓度___________
20.水解原理在生产和生活中都具有重要的用途.下列应用与盐类的水解无关的是( )
| A. | TiCl4溶于大量水加热制备TiO2 | |
| B. | 热的纯碱溶液用于清洗油污 | |
| C. | 次氯酸钠常用作消毒剂 | |
| D. | FeCl3饱和溶液滴入沸水中制Fe(OH)3胶体 |


 )在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
)在碱性条件下水解的装置图。进行皂化反应时的步骤如下:
 g氢氧化钠,5 mL水和10 mL酒精。加入酒精的作用是____________。
g氢氧化钠,5 mL水和10 mL酒精。加入酒精的作用是____________。 3)图中长玻璃导管的作用为_________________________。
3)图中长玻璃导管的作用为_________________________。