题目内容
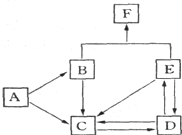
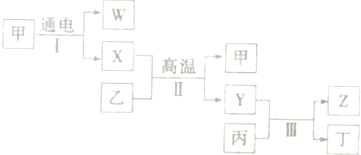
甲、乙、丙三种物质之间有如下转化关系:甲
乙
丙
甲
(1)若乙溶液中加入KSCN溶液,有红色出现,则甲物质是:______.写出“甲
乙”转化的离子方程式:______.
(2)若甲是不溶于水的白色粉末状物质,既能溶于盐酸又能溶于氢氧化钠溶液,则乙是______.写出“乙
丙”转化的化学方程式:______.
| 硫酸 |
| 氨水 |
| △ |
(1)若乙溶液中加入KSCN溶液,有红色出现,则甲物质是:______.写出“甲
| 硫酸 |
(2)若甲是不溶于水的白色粉末状物质,既能溶于盐酸又能溶于氢氧化钠溶液,则乙是______.写出“乙
| 氨水 |
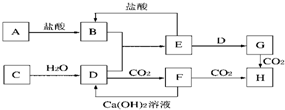
(1)若乙溶液中加入KSCN溶液,有红色出现,说明乙中含有Fe3+,加入氨水生成Fe(OH)3,加热分解生成Fe2O3,Fe2O3与硫酸反应的离子方程式为Fe2O3+6H+=2Fe3++3H2O,
故答案为:Fe2O3;Fe2O3+6H+=2Fe3++3H2O;
(2)若甲是不溶于水的白色粉末状物质,既能溶于盐酸又能溶于氢氧化钠溶液,应为两性化合物,可能为Al2(SO4)3或Al2O3,乙应为Al2(SO4)3,丙为Al(OH)3,则甲为Al2O3,Al2(SO4)3与氨水反应的化学方程式为Al2(SO4)3+6NH3?H2O=3(NH4)2SO4+2Al(OH)3↓,
故答案为:Al2(SO4)3;Al2(SO4)3+6NH3?H2O=3(NH4)2SO4+2Al(OH)3↓.
故答案为:Fe2O3;Fe2O3+6H+=2Fe3++3H2O;
(2)若甲是不溶于水的白色粉末状物质,既能溶于盐酸又能溶于氢氧化钠溶液,应为两性化合物,可能为Al2(SO4)3或Al2O3,乙应为Al2(SO4)3,丙为Al(OH)3,则甲为Al2O3,Al2(SO4)3与氨水反应的化学方程式为Al2(SO4)3+6NH3?H2O=3(NH4)2SO4+2Al(OH)3↓,
故答案为:Al2(SO4)3;Al2(SO4)3+6NH3?H2O=3(NH4)2SO4+2Al(OH)3↓.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目